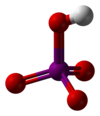
高碘酸
高碘酸是碘的最高含氧酸,其中碘以+7氧化态存在。它可以以两种形式存在:化学式为H5IO6的正高碘酸和化学式为HIO4的偏高碘酸。
| 高碘酸 | |||
|---|---|---|---|
| |||
| |||
 | |||
| 别名 | 碘(VII)酸 | ||
| 识别 | |||
| CAS号 | 10450-60-9(正高碘酸) 13444-71-8(偏高碘酸) | ||
| ChemSpider | 23622 (正高碘酸), 58684 (偏高碘酸) | ||
| SMILES |
| ||
| InChI |
| ||
| InChIKey | TWLXDPFBEPBAQB-UHFFFAOYSA-N | ||
| UN编号 | UN3085 | ||
| 性质 | |||
| 化学式 | HIO 4(偏高碘酸) H 5IO 6(正高碘酸) | ||
| 摩尔质量 | 190.91 g/mol (HIO 4) 227.941 g/mol (H 5IO 6) g·mol⁻¹ | ||
| 外观 | 无色晶体 | ||
| 熔点 | 128.5 °C(402 K)([1]) | ||
| 溶解性 | 溶于水、醇 | ||
| 危险性 | |||
GHS危险性符号    | |||
| GHS提示词 | Danger | ||
| H-术语 | H271, H314, H372, H400 | ||
| P-术语 | P210, P260, P273, P303+361+353, P305+351+338 | ||
| NFPA 704 | |||
| 相关物质 | |||
| 其他阴离子 | |||
| 其他阳离子 | |||
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |||
高碘酸由海因里希·古斯塔夫·马格努斯和CF Ammermüller于1833年发现。[2]
合成
现代工业规模生产涉及碘酸钠溶液在碱性条件下的氧化,或者在PbO
2阳极上进行电化学氧化,或者通过氯处理:[3]
- IO−
3 + 6 HO−
- 2 e−
→ IO5−
6 + 3 H
2O (为方便省略抗衡离子) E° = -1.6 V[4] - IO−
3 + 6 HO−
+ Cl
2 → IO5−
6 + 2 Cl−
+ 3 H
2O
原高碘酸在减压下加热至100℃可脱水得到偏高碘酸。
- H
5IO
6 ⇌ HIO
4 + 2 H
2O
进一步加热至约150 °C得到五氧化二碘(I
2O
5),而不是预期的酸酐[七氧化二碘(I
2O
7)]。偏高碘酸也可由各种正高碘酸盐经稀硝酸处理制得。[5]
性质
正高碘酸有多個酸解离常数。[6][7] 偏高碘酸的pKa尚未确定。
- H
5IO
6 ⇌ H
4IO−
6 + H+
, pKa = 3.29
- H
4IO−
6 ⇌ H
3IO2−
6 + H+
, pKa = 8.31
- H
3IO2−
6 ⇌ H
2IO3−
6 + H+
, pKa = 11.60
存在两种形式的高碘酸,因此形成两种类型的高碘酸盐。例如,偏高碘酸钠NaIO4可以由HIO4合成,而正高碘酸钠Na5IO6可以由H5IO6合成。
结构
正高碘酸形成单斜晶体(空间群P21/n),由一个轻微变形的IO
6八面体通过桥接氢相互连接组成。五个I-O键距离在1.87-1.91 Å范围内,一个I-O键距离为 1.78 Å。[8][9]偏高碘酸的结构还包括IO
6八面体,但是它们通过顺共棱与桥氧连接形成一维无限链。[10]
反应
像所有高碘酸盐一样,高碘酸可用于裂解各种1,2-双官能团化合物。高碘酸会将邻二醇裂解成两个醛或酮片段(马拉普拉德反应)。

这可用于确定碳水化合物的结构,因为高碘酸可用于打开糖环。该过程通常用于用荧光分子或其他标签(如生物素)标记糖类。由于该过程需要连位二醇,因此高碘酸盐氧化通常用于选择性标记RNA的 3'-末端(核糖具有连位二醇)而不是DNA,因为脱氧核糖没有连位二醇。
高碘酸也被用作中等强度的氧化剂,例如在仲烯丙醇的Babler氧化反应中,通过化学计量的正高碘酸与催化剂PCC将其氧化成烯酮。[11]
参见
具有相似结构的化合物:
化学性质相似的化合物: