四氟化氙
化合物
四氟化氙(化学式:XeF4)是稀有气体氙的氟化物之一,是第一个发现的稀有气体二元化合物。[2]
| 四氟化氙 | |||
|---|---|---|---|
 | |||
| |||
| IUPAC名 Xenon tetrafluoride | |||
| 别名 | 氟化氙(IV) | ||
| 识别 | |||
| CAS号 | 13709-61-0 | ||
| PubChem | 123324 | ||
| ChemSpider | 109927 | ||
| SMILES |
| ||
| InChI |
| ||
| InChIKey | RPSSQXXJRBEGEE-UHFFFAOYAW | ||
| 性质 | |||
| 化学式 | XeF4 | ||
| 摩尔质量 | 207.2836 g·mol⁻¹ | ||
| 外观 | 白色固体 | ||
| 密度 | 4.040 g/cm3 (固) | ||
| 升华条件 | 117 °C (390 K)[1] | ||
| 结构 | |||
| 配位几何 | D4h | ||
| 分子构型 | 平面正方形 | ||
| 偶极矩 | 0 D | ||
| 危险性 | |||
| 闪点 | ? °C | ||
| 相关物质 | |||
| 相关化学品 | 二氟化氙、六氟化氙 | ||
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |||
製造
- 首次制备的方法:由Xe与F2以1:2摩尔比反应得到。[3][4]该反应是放热反应,每摩尔反应放出251kJ的热量。[2]
- 放电合成法:将氙与氟按体积比1:2加入反应容器(温度需控制在-78℃),放电条件为1100V、31mA到2800V、12mA,反应历时3小时。电压不能太高否则氙与氟发生燃烧反应。为了主要获得四氟化氙,氟需要略微过量。
- 二氟化二氮氟化法:在200℃以下将二氟化二氮与氙共热,主要得到四氟化氙。该法可以避免使用危险且难以制备的氟单质。
物理性质
四氟化氙是一种无色固体,室温下易升华。四氟化氙微溶于无水氟化氢,但并不电离。它不溶于全氟庚烷中,但可溶于NOF·3HF。[5]
结构
1963年核磁共振谱与X射线晶体学数据显示其四氟化氙的空间构型为平面正方形。[6][7]四氟化氙为体心单斜晶系,X射线衍射法和中子衍射法测得Xe-F键键长约为190pm。
化学性质
四氟化氙在室温下稳定,可以长期储存在镍制容器中,如果去除水和氟化氢也可保存在玻璃容器中。
- 它能被氢气还原,该反应可用于分析鉴定:
- 这个反应机理很复杂,Xe(IV)先发生歧化反应得到Xe(0)和Xe(VI),然后分别氧化水并放出氧气。
- 它在撞击或震动下都很稳定,不会爆炸性分解。但与有机物(例如四氢呋喃、二氧六环、丙酮、乙烯)接触时会剧烈反应而引起燃烧。如果与气态的乙醇或丙酮反应将发生爆炸。
- 氟磺酸中的-OSO2F是电负性很高的基团,可取代四氟化氙中的氟原子形成衍生物:
- 但后来化学家再次进行该实验时,只得到了二氟化氙的衍生物。这可能是过去使用的四氟化氙不纯造成的。[5]
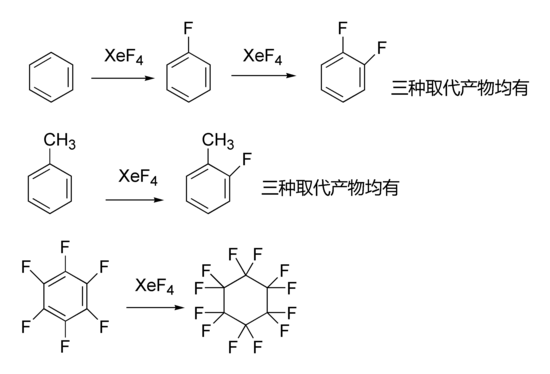
- 以下是四氟化氙参与的有机反应: