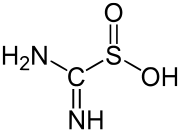
சல்பினிக் அமிலம்
சல்பினிக் அமிலங்கள் (Sulfinic acids) என்பவை கந்தகத்தின் ஆக்சோ அமிலங்களாகும். இவற்றினுடைய பொதுக் கட்டமைப்பு RSO(OH) என்று அமைகிறது. கரிமக் கந்தகச் சேர்மமான இச்சேர்மத்தில் கந்தகம் பட்டைக்கூம்பு வடிவத்தில் உள்ளது.
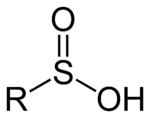
பெரும்பாலும் தொடர்புடைய சல்பினேட்டு உப்புகளை அமிலமாக்கல் முறையில் தளத்திலேயே இவை உற்பத்தி செய்யப்படுகின்றன. குறிப்பாக இவ்வுப்புகள் அமிலத்தைக் காட்டிலும் திடமானவையாகும். சல்போனைல் குளோரைடுகளை ஒடுக்குவதன் மூலம் இவ்வுப்புகள் தயாரிக்கப்படுகின்றன[1]. கிரிக்கனார்டு வினைப்பொருளை கந்தக டை ஆக்சைடுடன் வினைபுரியச் செய்து தயாரிப்பது ஒரு மாற்று வழிமுறையாகும். உலோக ஆல்கைல்களுக்கு இடையில் கந்தக டை ஆக்சைடை செருகுவதன் மூலம் இடைநிலை உலோக சல்பினேட்டுகள் உருவாகின்றன. இவ்வினை உலோக கந்தக டை ஆக்சைடு அணைவுத்தொகுதி வழியாக நிகழ்கிறது. R ஐதரசனாக உள்ள பதிலீடு செய்யப்படாத சல்பினிக் அமிலம், சல்பாக்சிலிக் அமிலத்தின் உயராற்றல் மாற்றியன் ஆகும். இவையிரண்டுமே நிலைத்தன்மை அற்றவைகளாகும்.
உதாரணங்கள்
பீனைல் சல்பினிக் அமிலம் ஒரு எளிய நன்கு ஆராயப்பட்ட சல்பினிக் அமிலமாகும். வர்த்தக ரீதியாக முக்கியத்துவம் பெற்ற சல்பினிக் அமிலம் தயோயூரியா டை ஆக்சைடு ஆகும். தயோயூரியாவை ஐதரசன் பெராக்சைடுடன் சேர்த்து ஆக்சிசனேற்றம் செய்வதனால் தயோயூரியா டை ஆக்சைடு உருவாகிறது [2]
- (NH2)2CS + 2H2O2 → (NH)(NH2)CSO2H + 2H2O
ஐதராக்சிமெத்தில் சல்பினிக் அமிலம் என்ற சேர்மமும் வர்த்தக முக்கியத்துவம் மிக்க ஒரு சேர்மமாகும். வழக்கமாக அதனுடைய ரோங்கலைட்டு எனப்படும் சோடியம் உப்பிலிருந்து (HOCH2SO2Na) இது தயாரிக்கப்படுகிறது. இவ்வுப்பின் எதிர்மின் அயனியும் ஒடுக்கும் முகவராக முக்கியத்துவம் பெறுகிறது.
சல்பினைட்டு
சல்பினிக் அமிலத்தினுடைய இணை காரமாக கருதப்படுவது சல்பினைட்டு எதிர்மின் அயனியாகும். சிசுட்டின் டையாக்சிசனேசு நொதி சிசுட்டினை தொடர்புடைய சல்பினைட்டாக மாற்றுகிறது. இவ்வளர்சிதை மாற்ற வினையில் ஐபோட்டாயூரின் என்ற சல்பினிக் அமில வழிப்பொருள் உருவாகிறது.