ஐதரசன் புரோமைடு
ஐதரசன் புரோமைடு (Hydrogen bromide ) என்பது HBr என்ற மூலக்கூற்று வாய்ப்பாடு கொண்ட ஓர் ஈரணு மூலக்கூற்றுச் சேர்மமாகும். நிறமற்ற நிலையில் இருக்கும் இவ்வாயு நிறமற்ற நீர்மமாகச் சுருங்குகிறது. ஐதரசன் புரோமைடு வாயு நீரில் கரைந்தால் ஐதரோபுரோமிக் அமிலம் உருவாகிறது. ஐதரசன் புரோமைடு மற்றும் ஐதரோ புரோமிக் அமிலம் என்பவை இரண்டும் வெவ்வேறானவை, ஆனால் ஒன்றுடன் ஒன்று தொடர்புள்ளவை. பொதுவாக வேதியியலாளர்கள் ஐதரோ புரோமிக் அமிலத்தைத்தான் "HBr" என்று குறிப்பிடுவார்கள். இப்பயன்பாடு வேதியல் வல்லுநர்களுக்கு எளிமையான புரிதலையும் மற்றவர்களுக்கு சிறிய குழப்பத்தையும் அளிக்கும்.
 | |||
| |||
| பெயர்கள் | |||
|---|---|---|---|
| விருப்பத்தெரிவு ஐயூபிஏசி பெயர் Hydrogen bromide[சான்று தேவை] | |||
| முறையான ஐயூபிஏசி பெயர் புரோமேன்[1] | |||
| இனங்காட்டிகள் | |||
| 10035-10-6 | |||
Beilstein Reference | 3587158 | ||
| ChEBI | CHEBI:47266 | ||
| ChEMBL | ChEMBL1231461 | ||
| ChemSpider | 255 | ||
| EC number | 233-113-0 | ||
| யேமல் -3D படிமங்கள் | Image | ||
| KEGG | C13645 | ||
| ம.பா.த | ஐதரோபுரோமிக்+அமிலம் | ||
| பப்கெம் | 260 | ||
| வே.ந.வி.ப எண் | MW3850000 | ||
| |||
| UN number | 1048 | ||
| பண்புகள் | |||
| BrH | |||
| வாய்ப்பாட்டு எடை | 80.91 g·mol−1 | ||
| தோற்றம் | நிறமற்ற வாயு | ||
| மணம் | கடுங்கார்ப்பு | ||
| அடர்த்தி | 3.6452 கி.கி/மீ3 (0 °செ, 1013 மில்லிபார்)[2] | ||
| உருகுநிலை | −86.9 °C (−124.4 °F; 186.2 K) | ||
| கொதிநிலை | −66.8 °C (−88.2 °F; 206.3 K) | ||
| 221 கி/100 மி.லி (0 °செ) 204 கி/100 மி.லி (15 °செ) 193 கி/100 மி.லி (20 °செ) 130 கி/100 மி.லி (100 °செ) | |||
| கரைதிறன் | ஆல்ககால், கரிமக் கரைப்பன்களில் கரையும் | ||
| ஆவியமுக்கம் | 2.308 மெகாபாசுகல் ( 21 °செ)இல் | ||
| காடித்தன்மை எண் (pKa) | ~–9[3] | ||
| காரத்தன்மை எண் (pKb) | ~23 | ||
| ஒளிவிலகல் சுட்டெண் (nD) | 1.325 | ||
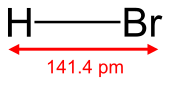
| கட்டமைப்பு | |||
| மூலக்கூறு வடிவம் | |||
| இருமுனைத் திருப்புமை (Dipole moment) | 820 mD | ||
| வெப்பவேதியியல் | |||
| Std enthalpy of formation ΔfH | -36.45--36.13 kJ mol−1[4] | ||
| நியம மோலார் எந்திரோப்பி S | 198.696-198.704 J K−1 mol−1[4] | ||
| வெப்பக் கொண்மை, C | 350.7 mJ K−1 g−1 | ||
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |||
நீரில் கரைதிறன்
ஐதரசன் புரோமைடு தண்ணீரில் நன்றாகக் கரைந்து ஐதரோபுரோமிக் அமிலத்தை உருவாக்குகிறது. அறை வெப்பநிலையில் அதன் எடையில் 68.85 சதவீதம் கரைந்தபிறகு நிறைவுற்ற கரைசலாகிறது. நீர்க்கரைசல்களில் 47.6 சதவீதம் ஐதரசன் புரோமைடு கரைந்துள்ளது. எடையை அடிப்படையாகக் கொண்டு உருவாகும் இதனுடைய கொதிநிலை மாறாக் கலவை 124.3 0 செல்சியசு வெப்பநிலையில் கொதிக்கிறது. அடர்த்தி குறைவான கரைசல்கள் கொதிநிலை மாறாக் கலவையின் இயைபை எட்டும் வரை தண்ணீரை வெளியேற்றுகின்றன.
பயன்கள்
கனிம மற்றும் கரிம புரோமின் சேர்மங்களை உற்பத்தி செயவதில் ஐதரசன் புரோமைடு மற்றும் ஐதரோபுரோமிக் அமிலம் ஆகியவை இரண்டும் முக்கியப் பங்காற்றுகின்ற வினைப்பொருட்களாகும்[5]. ஆல்க்கீன்களுடன் ஐதரசன் புரோமைடின் தனி உறுப்புச் சேர்க்கையால் விளிம்புநிலை ஆல்கைல் புரோமைடுகள் உருவாகின்றன.
- RCH=CH2 + HBr → RCH2–CH2Br
கொழுப்பு அமைன் வழிபொருட்களுக்கு இப்புரோமைடுகள் முன்னோடிகளாகத் திகழ்கின்றன. இதே போன்று அல்லைல் குளோரைடு மற்றும் பினித்தீனுடன் தனி உறுப்புச் சேர்க்கை வினையில் ஈடுபட்டு முறையே -1- புரோமோ -3- குளோரோபுரோப்பேன் மற்றும் பீனைல்யெத்தில்புரோமைடுகளை உருவாக்குகிறது.
இருகுளோரோமீத்தேனுடன் ஐதரசன் புரோமைடு வினைபுரிந்து வரிசை முறையாக புரோமோகுளோரோமீத்தேன் மற்றும் இருபுரோமோயீத்தேன்களை உருவாக்குகிறது.
- HBr + CH2Cl2 → HCl + CH2BrCl
- HBr + CH2BrCl → HCl + CH2Br2
அல்லைல் ஆல்ககாலுடன் ஐதரசன் புரோமைடு சேர்த்து வினைப்படுத்தினால் அல்லைல்புரோமைடு தயாரிக்கலாம்.
- CH2=CHCH2OH + HBr → CH2=CHCH2Br + H2O
இதர வினைகள்
தொழிற்சாலைகளில் ஐதரசன் புரோமைடு பரவலாகப் பயன்படுத்தப்படுவதில்லை என்றாலும் ஆல்க்கீன்களுடன் சேர்க்கப்பட்டு புரோமோ ஆல்க்கீன்கள் தயாரிக்கப்படுகின்றன. இவை மிகமுக்கியமான கரிமபுரோமின் வகைச் சேர்மங்கள் குடும்பமாகும். அவ்வாறே ஆலோ ஆல்க்கீன்களுடன் HBr சேர்ந்து ஒரிடத்த ஈராலோ ஆல்க்கேன்களை தோற்றுவிக்கிறது. இச்சேர்க்கைகள் மார்க்கோணிக்காவ் விதியைப் பின்பற்றுகின்றன.
- RC(Br)=CH2 + HBr → RC(Br2)–CH3
HBr ஆல்க்கைன்களுடன் சேர்ந்தும் புரோமோ ஆல்க்கீன்களைத் தருகின்றன. பொதுவாக இவ்வகையான சேர்க்கைகள் முப்பரிமான வேதியியலுக்கு எதிரானவையாகும்.
- RC≡CH + HBr → RC(Br)=CH2
மேலும், ஈப்பாக்சைடுகள் மற்றும் லாக்டோன்கள் திறப்பிலும் தொகுப்பு முறையில் புரோமோ அசிட்டால்களைத் தயாரிப்பதிலும் ஐதரசன் புரோமைடு பயன்படுகிறது. தவிர பல கரிம வினைகளில் HBr வினையூக்கியாகவும் செயல்படுகிறது.[6][7][8][9]
சாத்தியமுள்ள பயன்கள்
மின்கலன்களில் பயன்படுத்துவதற்கு HBr பரிந்துரைக்கப்பட்டு வருகிறது.[10]
தொழில்முறை தயாரிப்பு
ஐதரசன் மற்றும் புரோமின் வாயுக்களை 200-400 °செ வெப்பநிலையில் பிளாட்டின வினையூக்கி அல்லது கல்நார் முன்னிலையில் சேர்த்து ஐதரசன் புரோமைடும் ஐதரோபுரோமிக் அமிலமும் தயாரிக்கப்படுகின்றன.[7][11]
ஆய்வகத் தயாரிப்பு முறைகள்
ஐதரசன் புரோமைடு ஆய்வகத்தில் பல்வேறு வழிமுறைகளில் தயாரிக்கப்படுகின்றது. சோடியம் புரோமைடு அல்லது பொட்டாசியம் புரோமைடுடன் பாசுபாரிக் அமிலம் அல்லது நீர்த்த கந்தக அமிலம் சேர்த்து காய்ச்சி வடித்தால் ஐதரசன் புரோமைடு உண்டாகிறது.:[12]
- 2 KBr + H2SO4 → K2SO4 + 2HBr
அடர் கந்தக அமிலம் இதற்குப் பயன்படாது ஏனெனில் ஐதரசன் புரோமைடை அது உருவானவுடன் புரோமின் வாயுவாக ஆக்சிசனேற்றம் செய்து விடுகிறது.
- 2 HBr + H2SO4 → Br2 + SO2 + 2H2O
ஐதரோபுரோமிக் அமிலத்தையும் பலவழிகலில் தயாரிக்க முடியும். புரோமினை பாசுபரசு மற்றும் நீருடன் சேர்த்து அல்லது கந்தகம் மற்றும் நீருடன் சேர்த்து இதைத் தயாரிக்கலாம்:[12].
- 2 Br2 + S + 2 H2O → 4 HBr + SO2
டெட்ராலினை புரோமினேற்றம் செய்தும் மாற்றுவழியில் ஐதரோபுரோமிக் அமிலத்தைத் தயாரிக்கலாம்:[12].
- C10H12 + 4 Br2 → C10H8Br4 + 4 HBr
புரோமினுடன் பாசுபரசமிலத்தைச் சேர்த்து வினைப்படுத்தியும் இதைத் தயாரிக்கமுடியும்:[7].
- Br2 + H3PO3 + H2O → H3PO4 + 2 HBr
முப்பீனைல்பாசுபோனியம்புரோமைடை எதிரொழுக்கு சைலீனுடன் வெப்பமுறிவு வினையில் ஈடுபடுத்தினால் ஐதரசன் புரோமைடின் நீரிலி வடிவம் கிடைக்கிறது.[6]மேற்கண்ட முறைகளில் தயாரிக்கப்படும் ஐதரசன் புரோமைடானது புரோமின் வாயுவினால் மாசடைந்து காணப்படுகிறது. எனவே இவ்வயுக் கலவையை அறை வெப்ப நிலையில் நாற்குளோரோமீத்தேனில் உள்ள பீனால் அல்லது பொருத்தமான வேறு கரைப்பானின் (2,4,6-முப்புரோமோபீனால் பயன்படுத்தினால் கூடுதலாக HBr கிடைக்கும்) வழியாகச் செலுத்தி தூய்மைப்படுத்தலாம். உயர் வெப்பநிலைகளில் தாமிரத் துருவல்கள் வழியாகச் செலுத்தியும் தூய்மைப்படுத்தலாம்.[11]
பாதுகாப்பு
ஐதரசன் புரோமைடு அரிப்புத் தன்மை கொண்டது என்பதால் சுவாசிக்க நேரிட்டால் தீங்கை விளைவிக்கும்.

