Наследни ангиоедем
Наследни ангиоедем или хередитарни ангиоедем (акроним ХАЕ) се карактерише рекурентним епизодама локализованих едема (отока) коже и слузокоже гастроинтестиналног, урогениталног и респираторног тракта. Настаје као последица наследног недостатка или снижених вредности инхибитора Ц1 естеразе, због чега настају дефекти у систему комплемента.[4]
| Наследни ангиоедем | |
|---|---|
| Синоними | Hereditary angioneurotic edema (HANE),[1] familial angioneurotic edema[2] |
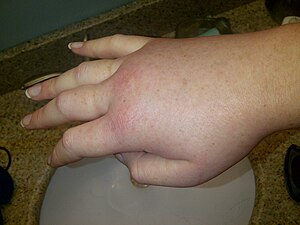 | |
| Отечена десна рука током наследног напада ангиоедема. | |
| Специјалности | хематологија |
| Симптоми | понављајући ангиоедем[3] |
| Време појаве | детињство[3] |
| Трајање | напади трају по неколико дана[3] |
| Типови | Тип I, II, III[3] |
| Узроци | генски поремећај (аутозомно доминантан)[3] |
| Дијагностички метод | Мерење нивоа C4 и C1-инхибитора.[2] |
| Слична обољења | интестинална опструкција, други типови ангиоедема[2] |
| Превенција | C1 инхибитор[3] |
| Лечење | медицинска подршка, лекови[1] |
| Лекови | C1 инхибитор, ecallantide, icatibant[1] |
| Прогноза | 25% ризик од смрти ако су захваћени дисајни путеви (без лечења)[2] |
| Фреквенција | ~1 у 50.000[3] |
Мања траума или стрес могу изазвати напад, али оток се често јавља и без познатог окидача. Епизоде које захватају цревни тракт изазивају јак бол у трбуху, мучнину и повраћање. Отицање дисајних путева може ограничити дисање и довести до опструкције дисајних путева опасне по живот. Отприлике једна трећина људи са овим стањем током напада развије осип који не сврби и носи назив назив еритема маргинатум.[5]
Епидемиологија
Процењује се да наследни ангиоедем погађа 1 од 50.000 људи,[6] до 1-9 од 100.000.[7][8]
Тип I је најчешћи и чини 85% случајева. Тип II се јавља у 15 одсто случајева, а тип III се јавља јако ретко.[6]
Наслеђе
Ово стање се наслеђује аутозомно доминантно, што значи да је једна копија измењеног гена у свакој ћелији довољна да изазове поремећај.[9]
У неким случајевима, оболела особа наследи мутацију од једног захваћеног родитеља . Други случајеви су резултат нових мутација гена и јављају се код људи који немају историју поремећаја у својој породици.[9]
Етиопатогенеза
Наследни ангиоедем је вероватно аутозомно доминантно наследан поремећај, у коме су као етиолошки фактори доминантни:[10]
- трауматизам (ОРЛ или стоматолошке интервенције),
- неки инфекције,
- физички напор,
- стрес,
- лекови.
Генетика
Мутације у СЕРПИНГ1 гену[11][12] - узрокују наследни ангиоедем типа I и типа II . СЕРПИНГ1 ген даје упутства за стварање протеина инхибитора Ц1,[13] који је важан за контролу упале. Ц1 инхибитор блокира активност одређених протеина који подстичу упалу. Мутације које изазивају наследни ангиоедем типа I доводе до смањеног нивоа Ц1 инхибитора у крви, док мутације које изазивају ангиоедем тип II доводе до производње Ц1 инхибитора који функционише абнормално. Без одговарајућих нивоа функционалног инхибитора Ц1, стварају се превелике количине протеинског фрагмента (пептида) званог брадикинин. Брадикинин подстиче упалу повећавајући цурење течности кроз зидове крвних судова у телесна ткива. Прекомерна акумулација течности у телесним ткивима изазива епизоде отока који се примећују код особа са наследним ангиоедемом типа I и типа II.[14]
Мутације у гену Ф12 - су повезане са неким случајевима наследног ангиоедема типа III. Овај ген даје упутства за стварање протеина који се зове фактор коагулације XII. Поред тога што игра критичну улогу у згрушавању крви (коагулацији), фактор XII је такође важан стимулатор упале и укључен је у производњу брадикинина. Одређене мутације у гену Ф12 резултују производњом фактора XII са повећаном активношћу. Као резултат тога, ствара се више брадикинина и зидови крвних судова постају пропуснији, што доводи до епизода отока код људи са наследним ангиоедемом типа III.
Узрок других случајева наследног ангиоедема типа III остаје непознат. Мутације у једном или више још неидентификованих гена могу бити одговорне за поремећај у овим случајевима.[15]
Стечени ангиоедем се такође може јавити због имунолошких поремећаја, као што је су:[16]
- лимфопролиферативна болест Б-ћелија
- хроничне лимфоцитне леукемије,
- мултиплог мијелома,
- лупуса (СЛЕ),
- хроничног синуситиса,
- инфекције зуба
- одређени поремећаја крви (есенцијалне криоглобулинемије).
Други стечени едеми могу настати због операције (мастектомије), малигнитета и/или аутоимуних болести.[16]
Стечени ангиоедем се може јавити у било ком узрасту.[16]
Клиничка слика

Почетак клиничке слике се може јавити у било ком узрасту, али је најчешћи у детињству или адолесценцији.
Пацијенти се јављају лекару са белим, ограниченим непруритским едемима који остају у периоду од 48 до 72 сата и понавља се са променљивом учесталошћу.[7]
Едеми могу захватити дигестивни тракт што резултује клиничком сликом сличном оној која се види код синдрома интестиналне оклузије, понекад удружене са асцитесом и хиповолемијским шоком.[7]
Едем ларинкса може бити опасан по живот са ризиком од смрти од 25% у одсуству одговарајућег лечења.[17] Стоматолошке процедуре су често окидач за едем ларинкса. Едеми лица је такође један од фактор ризика за захваћеност ларинкса.[7]
Дијагноза
Постављање дијагнозе генетске или ретке болести често може бити изазовно. Дијагноза наследног ангиоедема поставља се:[16]
- темељном клиничком проценом,
- детаљном анамнезом пацијента и детањно узете медицинске историје болести,
- симптома болести,
- лабораторијским тестовима и других тестова.
- генетским тестирањем (ГТР) које пружа информације о генетском статусу, уз консултацију са стручњаком за генетику.
Дијагноза типова I и II наследног ангиоедема заснива се на мерењу концентрације Ц4 и на квантитативној и функционалној анализи Ц1-ИНХ.[7]
Дијагноза наследног ангиоедема типа III се врти око препознавања клиничке слике; Нивои Ц4 и Ц1-ИНХ су нормални.[7]
Може се предложити анализа за мутације у гену Ф12, али су оне присутне код само 15% пацијената.[7]
У случајевима велике клиничке сумње и рекурентног епизодног ангиоедема неизвесне етиологије, индиковано је генетско тестирање.[16]
Диференцијална дијагноза
Диференцијална дијагноза треба да обухвати:[7][4]
- стечени ангиоедем,
- идиопатски ангиоедем,
- синдром интестиналне оклузије и
- хистамином изазван ангиоедем (алергеног или неалергеног порекла) генерално повезан са уртикаријом.
Препоручује се скрининг чланова породице, укључујући асимптоматске особе.
Терапија

Антихистаминици и други третмани који се користе користе за лечење ангиоедем не дају добре резултате код наследног ангиоедема. Епинефрин (адреналин) треба користити у реакцијама опасним по живот.[18]

Код велике већине пацијената са наследним ангиоедемом, напади ангиоедема су последица квантитативног или функционалног недостатка инхибитора Ц1-естеразе (Ц1-ИНХ), што доводи до повећане васкуларне пермеабилности и нерегулисаног ослобађања брадикинина.[19] Егзогена примена Ц1-ИНХ је рационалан начин да се поврати концентрација и функционална активност овог протеина, регулише ослобађање брадикинина и ублажи или спречи поткожни и субмукозни едем повезан са наследним ангиоедемом. Недавне међународне смернице за лечење наследног ангиоедемом укључују Ц1-ИНХ као опцију за акутни третман наследног ангиоедема . Поред тога, ове смернице препоручују Ц1-ИНХ као третман прве линије за дуготрајну профилаксу и као терапију избора за краткорочну/препроцедуралну профилаксу. [20]
Постоји и низ новијих третмана за наследни ангиоедем које је одобрила Америчка агенција за лекове и храну. Међу лековима из ове група спадају;[21]
- Цинризе,
- Беринерт,
- Руконест,
- Калбитор и
- Фиразир.
- Беротралстат, који се препоручује као опција за превенцију рекурентних напада наследног ангиоедема код особа старијих од 12 година, само ако: имају најмање 2 напада месечно, а прекида се ако се број напада месечно не смањи за најмање 50% после 3 месеца.[22] Упркос извесној несигурности у клиничким доказима, беротралстат се сматра исплативим за људе који имају најмање два напада месечно. Дакле, препоручује се за ове пацијенте.[22]
Неки се дају кроз вену (ИВ) и могу се користити и код куће. Други се пацијенту даје као инјекција под кожу. Избор агенса може бити заснован на старости особе и месту појаве симптома
Пре него што су ови новији лекови постали доступни, андрогени лекови, као што је даназол, коришћени су за смањење учесталости и тежине напада. Ови лекови помажу телу да производи више Ц1 инхибитора. Међутим, многе жене имају озбиљне нежељене ефекте од ових лекова. Такође се не могу користити код деце.
Када дође до напада, лечење укључује ублажавање болова и унос течности које се дају кроз вену интравенском (ИВ) линијом.

Хеликобактер пилори (лат. Helicobacter pylori), је врста бактерије која се налази у трбуху болесника, а за коју се сматра да узрочник уртикарије и ангиоедема.[23] Међународна испитивања, утврдила су да се број честих, едематозних абдоминалних напада може значајно смањити након ерадикације хеликобактер пилори код пацијената са наследним ангиоедемом инфицираним овим патогеном. Стога се чини да је скрининг пацијената са наследним ангиоедемом на инфекцију хеликобактер пилори оправдан. У том смислу антибиотици за лечење бактерија помажу у редукцији абдоминалних напада ангиоедема и значајно смањењују тежину болести.[24]
Брига о деци која болују од наследног ангиодема:
За децу су потребни индивидуални планови лечења, који подлежу редовном прегледу. Хитни лекови морају бити доступни за школска путовања, распусте, итд. Наставници, чувари деце, итд, требају да поседују адекватне информације о стању и лечењу акутних напада наследног ангиоедема.
Трудноћа
- Труднице треба да буду под надзором специјалисте за наследни ангиодем
- Дијагностичке тестове у трудноћи треба тумачити са опрезом јер се нивои Ц1-ИНХ мењају током трудноће.
- Акутне нападе треба лечити Ц1-ИНХ.
- Профилакса Ц1-ИНХ је најсигурнија.
- Лечење ослабљеним андрогенима је контраиндиковано (осим краткотрајне профилаксе у трећем триместру).
- Може се размотрити примена транексамске киселине, али ефикасност није доказана.
- Концентрате Ц1-ИНХ такође треба користити за препроцедуралну профилаксу током трудноће.[25]
Профилакса
Дуготрајна профилакса
Дугорочну профилаксу треба размотрити код пацијената са честим нападима, нарушеним квалитетом живота или недостатком контроле болести уз помоћ терапије ублажавања симптома. У Немачкој су за ову сврху одобрени концентрати Ц1-ИНХ (у вену и поткожно) и каликреинско антитело ланаделумаб.[26][27]
У прошлости су се често користили мушки полни хормони (андрогени), који повећавају производњу Ц1-ИНХ у јетри преко механизма који још увек није разјашњен. Употреба андрогена је контраиндикована код деце, као и у трудноћи и код жена које желе да имају децу. Вишеструка појава тумора јетре под андрогеном даназолом довело до тога да је супстанца искључена са тржишта у Немачкој почетком 2005. године.[28]
АЦЕ инхибиторе треба заменити антихипертензивним лековима који не повећавају брадикинин.
Краткорочна профилакса
Краткорочна профилакса се обично спроводи пре операције или лечења зуба. У Немачкој се концентрат Ц1-ИНХ даје 1-1½ сата пре процедуре. У земљама у којима није доступан концентрат инхибитора Ц1 за профилаксу, лечење високим дозама андрогена се спроводи током пет до седам дана.
Прогноза
Витална прогноза је добра за пацијенте којима је правовремено постављена дијагноза и који имају приступ одговарајућем лечењу у случају едема уха-носа-грла.[7]
Значајан морбидитет може бити повезан са захваћеношћу дигестивног система што доводи до бола и пацијената везују за кревет најмање три дана након епизоде.[7]
Нови и будући третмани
Инхибитор каликреина екалантид (Калбитор®, раније ДКС-88) који је одобрен за употребу у Сједињеним Америчким Државама (али не и за употребу у Европи), коридти се у нападима наследног ангиоедема, уопркос томе што код овог лека постоји ризик од анафилаксе.
Још један нови инхибитор каликреина показао је ефикасност у испитивањима и одобрен је у Сједињеним Америчким Државама.[29] То је Ланаделумаб ( људско моноклонско антитело) које циља на каликреин и спречава производњу брадикинина. Примјењује се субкутано. Тренутно овај лек нема дозволу за стављање у промет у Уједињеном Краљевству за спречавање напада ангиоедема код наследног ангиоедема, али је проучаван у испитивањима код људи старијих од 12 година или више који имају најмање један напад сваке четири недеље. Лек се разматра као могућу опција за профилаксу и пролази кроз даља испитивања.[24]
Друштво и култура
Постоје национална удружења за пацијенте са наследним ангиоедемом и њихове породице у великом броју земаља широм света. Ова национална удружења су чланови глобалне организације ХАЕи – Међународне организације пацијената за недостатке Ц1-инхибитора (енг. HAEi - International Patient Organization for C1-Inhibitor Deficiencies).[30]
Међународне организације пацијената за недостатке Ц1-инхибитора је посвећен подизању свести о недостацима инхибитора Ц1 широм света. То је непрофитна међународна мрежа основана да промовише сарадњу, координацију и размену информација између специјалиста за наследни ангиоедем и националних Удружења пацијената са наследним ангиоедемом како би се олакшала доступност ефикасне дијагнозе и управљања недостацима Ц1 инхибитора широм света.[30]
The Assistance Fund Inc је америчка непрофитна организација која нуди помоћ при плаћању за лекове који лече наследни ангиоедем и отворена је за све америчке грађане или имигранте који имају осигурање.
Лиса Сандерс је једном описала случај у својој колумни у The New York Times-у о мистериозном случају наследног ангиоедема изазваног контрацептивним пилулама.[31]
Извори
Спољашње везе
| Класификација | |
|---|---|
| Спољашњи ресурси |
 | Молимо Вас, обратите пажњу на важно упозорење у вези са темама из области медицине (здравља). |



