Natrijev hidrogenkarbonat
Natrijev hidrogenkarbonat, tudi ali natrijev bikarbonat, soda bikarbona ali bikarbona[7], je sol, tvorjena iz natrija in hidrogenkarbonata. Ker nastane v reakciji nevtralizacije iz natrijevega hidroksida, ki je močna baza, in šibke ogljikove kisline, izkazuje bazičen pH (okoli 9) in zato reagira s kislinami (reakcija kislin s karbonati) zelo burno, pri tem pa nastanejo sol (natrij + nekovina), ogljikov dioksid (CO2) in voda (H2O). Reakcija kislin z natrijevim hidrogenkarbonatom lahko poteče v vodni raztopini in pa v trdnem agregatnem stanju.
 | |||
| |||
 | |||
| Imena | |||
|---|---|---|---|
| IUPAC ime Natrijev hidrogenkarbonat | |||
| Druga imena soda bikarbona, natrijev bikarbonat | |||
| Identifikatorji | |||
3D model (JSmol) | |||
Beilstein | 4153970 | ||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| DrugBank | |||
| ECHA InfoCard | 100.005.122 | ||
| EC število |
| ||
| Število E | E500(ii) (sredstva za uravnavanje Ph, ...) | ||
| KEGG | |||
| MeSH | Sodium+bicarbonate | ||
PubChem CID | |||
| RTECS število |
| ||
| UNII | |||
CompTox Dashboard (EPA) | |||
| |||
| |||
| Lastnosti | |||
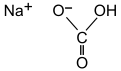
| NaHCO 3 | |||
| Molska masa | 84,007 g mol−1 | ||
| Videz | beli kristali | ||
| Vonj | brez vonja | ||
| Gostota | 2,20 g cm−3[1] | ||
| Tališče | 50 °C (122 °F; 323 K) | ||
| 9 g/100 mL 69 g/L (0 °C)[2] | |||
| Topnost | aceton: 0,02 %wt, metanol: 2,13 %wt pri 22 °C[4]. netopen v etanolu | ||
| log P | -0.82 | ||
| Kislost (pKa) | 10,329[5] 6,351 (ogljikova kislina)[5] | ||
| Lomni količnik (nD) | 1,3344 | ||
| Farmakologija | |||
| Aplikacija zdravila | intravensko, peroralno | ||
| Termokemija | |||
| Standardna molarna entropija S | 102 J·mol−1·K−1[6] | ||
Std tvorbena entalpija (ΔfH⦵298) | −948 kJ·mol−1[6] | ||
| Nevarnosti | |||
| Glavne nevarnosti | Povzroča hudo draženje oči. | ||
| NFPA 704 (diamant ognja) | |||
| Smrtni odmerek ali koncentracija (LD, LC): | |||
LD50 (srednji odmerek) | 4,22 g kg−1 | ||
| Sorodne snovi | |||
| Drugi anioni | natrijev karbonat | ||
| Drugi kationi | amonijev hidrogenkarbonat | ||
| Sorodne snovi | natrijev hidrogensulfat natrijev hidrogenfosfat | ||
Če ni navedeno drugače, podatki veljajo za material v standardnem stanju pri 25 °C, 100 kPa). | |||
| Sklici infopolja | |||
Sol je ena redkih hidrogenkarbonatov, ki so topni v vodi, sicer pa je njena topnost precej majhna.
Pri segrevanju razpade na natrijev karbonat (Na2CO3), vodo (H2O) in ogljikov(IV) oksid (CO).
- 2NaHCO3 → Na2CO3 + CO2 + H2O
Sproščeni plin je "kriv" za vzhajanje testa in rahlost peciv.
Je glavna sestavina pecilnega praška.
Uporaba
Kot zdravilo
Natrijev hidrogenkarbonat se uporablja kot antacid (nevtralizira želodčno kislino)[8] ter kot sredstvo proti presnovni acidozi[7].
Za nevtraliziranje želodčne kisline se uporablja natrijev hidrogenkarbonat peroralno (z zaužitjem). V želodcu nevtralizira kislino in s tem oblaži zgago, dispepsijo in slabost zaradi prekomerne kislosti želodčnega soka. Primeren je za kratkotrajno lajšanje težav.[9]
Pri presnovni acidozi se uporablja parenteralno. Delovanje izhaja iz njegove fiziološke vloge v puferskem sistemu HCO3ˉ/CO2. V telo vnesen natrijev hidrogenkarbonat hitro absorbira vodikove ione iz zunajceličnega prostora in tako povzroči zvišanje pH v organizmu in tudi seč se naalkali. Pri reakciji med hidrogenkabonatnim anionom in vodikovim kationom nastane ogljikov dioksid, ki se izloči z dihanjem. Zaradi naalkaljenja seča se lahko natrijev hidrogenkarbonat daje tudi pri zastrupitvi s šibkimi organskimi kislinami (npr. barbiturati ali acetilsalicilno kislino), za izboljšanje topnosti zdravilnih učinkovin, ki so težko topne v nevtralnih ali kislih medijih (npr. metotreksat, sulfonamidi) in za naalkaljenje urina v primeru hemolize.[10]


