Aluminijev nitrid
Aluminijev nitrid je spojina aluminija in dušika s formulo AlN. Njegova vurcitna faza (v-AlN) je polprevodnik s širokim prepovedanim pasom, pri sobni temperaturi 6,01-6,05 eV, in možno uporabnostjo v daljnji ultravijolični optični elektroniki.
 | |
 | |
| Identifikatorji | |
|---|---|
3D model (JSmol) | |
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard | 100.041.931 |
| EC število |
|
PubChem CID | |
| RTECS število |
|
CompTox Dashboard (EPA) | |
| |
| |
| Lastnosti | |
| AlN | |
| Molska masa | 40,9882 g/mol |
| Videz | bela do bledo rumena trdnina |
| Gostota | 3,260 g/cm3 |
| Tališče | 2.200 °C (3.990 °F; 2.470 K) |
| Vrelišče | 2.517 °C (4.563 °F; 2.790 K) |
| uprašen z vodo raegira, monokristaliničen je netopen | |
| Topnost | z etanolom reagira |
| Prepovedani pas | 6,015 eV [2] |
| Mobilnost elektronov | ~300 cm2/(V·s) |
| Toplotna prevodnost | 285 W/(m·K) |
| Lomni količnik (nD) | 1,9 – 2,2 |
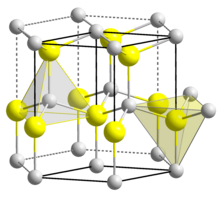
| Struktura | |
| Kristalna struktura | heksagonalna |
| Prostorska skupina | C6v4-P63mc |
| Koordinacijska geometrija | tetraedrična |
| Termokemija | |
| Specifična toplota, C | 30,1 J/mol K |
| Standardna molarna entropija S | 20,2 J/mol K |
Std tvorbena entalpija (ΔfH⦵298) | 318 kJ/mol |
Gibbsova prosta energija (ΔfG˚) | 287,4 kJ/mol |
| Nevarnosti | |
| NFPA 704 (diamant ognja) | |
Če ni navedeno drugače, podatki veljajo za material v standardnem stanju pri 25 °C, 100 kPa). | |
| Sklici infopolja | |
Zgodovina
Aluminijev nitrid so prvič sintetizirali leta 1877. Njegovo uporabnost v mikroelektroniki zaradi relativno visoke toplotne prevodnosti za električno izolacijsko keramiko so odkrili šele v 1980. letih. Toplotna prevodnost polikristaliničnega nitrida je 70–210 W•m−1•K−1, posameznih kristalov pa celo 285 W•m−1•K−1. [3]
Kemijske lastnosti
Aluminijev nitrid je v inertni atmosferi stabilen tudi pri visokih temperaturah in se pri 2800 °C raztali. V vakuumu pri ~1800 °C razpade. Na zraku začne pri 700 °C na površini oksidirati. 5-10 nm debel površinski sloj oksidov lahko nastane že pri sobni temperaturi in ščiti snov pred nadaljnjo oksidacijo do temperature 1370 °C. Nad to temperaturo se začne splošna oksidacija. V atmosferi vodika ali ogljikovega dioksida je obstojen do 980 °C.[4]
V anorganskih kislinah se počasi raztaplja, najprej na mejnih ploskev med zrni, v močnih alkalijah pa se raztapljajo zrna nitrida. V vodi počasi hidrolizira. Odporen je na taline večine soli, vključno s kloridi in kriolitom.
Proizvodnja
AlN se proizvaja z redukcijo aluminijevega oksida z ogljikom pri visoki temperaturi ali z neposrednim nitriranjem aluminija. Z dodatki za sintranje, kakršna sta Y2O3 ali CaO, in vročim stiskanjem nastane gost, tehnično uporaben material.
Uporaba
Aluminijev nitrid se uporablja predvsem v
- optični elektroniki
- dielektričnih slojih v optičnih medijih za shranjevanje podatkov
- elektronskih substratih in nosilcih čipov, kjer je bistvena visoka toplotna prevodnost
- vojaških aplikacijah
- talilnih lončkih za rast kristalov galijevega arzenida
- proizvodnji jekla in polprevodnikov
