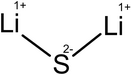
Сульфид лития
Сульфи́д ли́тия, сернистый литий — Li2S, неорганическое бинарное соединение, литиевая соль сероводородной кислоты.
| Сульфид лития | |||
|---|---|---|---|
| |||
| Общие | |||
| Систематическое наименование | Сульфид лития | ||
| Хим. формула | Li2S | ||
| Рац. формула | Li2S | ||
| Физические свойства | |||
| Состояние | твёрдое | ||
| Молярная масса | 45,95 г/моль | ||
| Плотность | 1,66[1] | ||
| Термические свойства | |||
| Температура | |||
| • плавления | 950[1] | ||
| • кипения | 1527[2] °C | ||
| Энтальпия | |||
| • образования | −447[3] кДж/моль | ||
| Классификация | |||
| Рег. номер CAS | 12136-58-2 | ||
| PubChem | 10290727 и 139047380 | ||
| Рег. номер EINECS | 235-228-1 | ||
| SMILES | |||
| InChI | |||
| RTECS | OJ6439500 | ||
| ChemSpider | 8466196 | ||
| Безопасность | |||
| Токсичность | ирритант | ||
| NFPA 704 | |||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
Физические свойства
Сульфид лития представляет собой светло-жёлтое[1] или бесцветное кристаллическое вещество[4], характеризующееся гранецентрированной кубической решёткой типа флюорита[5] (a = 0,571 нм, z = 4, пространственная группа Fm3m[6]), хорошо растворимое в воде, растворимое в спирте. Не образует кристаллогидратов.
Основные термодинамические характеристики[3]:
- стандартная энтальпия образования, ΔHo298 = −447 кДж/моль;
- стандартная энтропия образования, So298 = 63 Дж/(моль·K);
- стандартная энергия Гиббса образования, ΔGo298 = −439 кДж/моль.
Химические свойства
- Пропуская через водный раствор сероводород, реакцию гидролиза можно сместить вправо:
- Образующийся сильно гигроскопичный гидросульфид лития можно выделить в чистом виде[5].
- Водный раствор под действием кислорода воздуха на холоде постепенно окисляется, образуя осадок элементарной серы:
- Во влажном воздухе вещество постепенно окисляется до тиосульфата[4]:
- При действии окислителей (O2, KClO3, PbO2 и пр.) при нагревании свыше 300 °C сульфид лития окисляется до сульфата[1]:
- Вступает в реакции с разбавленными кислотами с выделением сероводорода:
- Являясь сильным восстановителем, с концентрированными серной и азотной кислотами, сульфид лития вступает в окислительно-восстановительные реакции:
Получение
Одна из потенциальных проблем при получении сульфида лития заключается в легкости его окисления, особенно в присутствии воды. Кроме того, вследствие гидролиза препаративные методы, основанные на реакциях обмена в водных растворах, обычно непригодны.
Так как сульфид лития не встречается в природе в виде минерального сырья, существуют следующие промышленные способы его получения[1][7]:
- взаимодействие гидрида лития с элементарной серой при температуре 300-350 °C:
- прокаливание оксида или карбоната лития в токе сухого сероводорода при температуре 900-1000 °C:
- восстановление сульфата лития коксом или водородом при высоких температурах:
Среди прочих возможных методов производства можно отметить[9]:
- взаимодействие гидроксида лития с газообразной серой при температуре до 445 °C:
- взаимодействие гидроксида лития с сероводородом в среде апротонного органического растворителя:
Полисульфиды лития
Для лития, в отличие от других щелочных металлов, полисульфиды не являются характерными соединениями и их получение требует особых условий[5][10].
Наиболее изучены[5]: 

 |  |
 |  |
Применение
Сульфид лития входит в состав анодов[11] и твёрдого электролита для литиевых элементов питания (батареек и аккумуляторов)[12]. Также используется как депиляционный агент в косметических средствах[13].
Может использоваться как компонент в производстве стёкол с высокой ионной проводимостью[14].
В современной органической химии сульфид лития иногда используется в качестве сульфидирующего агента, например, в следующей реакции[15]:
Также имеются данные об использовании этого вещества в качестве катализатора при защите гидроксильных групп через получение триметилсилилового эфира[16].
Потенциальная опасность для здоровья
Опасность для здоровья сульфида лития Li2S определяется как токсичностью ионов лития (Li+) из-за хорошей растворимости соединения в воде, так и токсичностью сероводорода, образующегося вследствие гидролиза этой соли.
Литий (в очень больших концентрациях), судя по всему, поражает центральную нервную систему, вызывая тремор рук, тошноту, повышенное мочеиспускание, нечленораздельность речи, вялость, сонливость, головокружение, жажду. Эффекты от длительного воздействия — апатия, анорексия, утомляемость, летаргия, мышечная слабость, изменения в ЭКГ. Долговременное токсическое действие вызывает гипотиреоз, лейкоцитоз, отёк и увеличение веса, полидипсию/полиурию, нарушение памяти, конвульсии, почечную недостаточность, шок, гипотонию, сердечные аритмии, кому, а также - летальный исход[17].
Литература
- Ахметов Н. С. Общая и неорганическая химия. — М.: Высшая школа, 2001. — ISBN 5-06-003363-5.
- Лидин Р. А. Справочник по общей и неорганической химии. — М.: КолосС, 2008. — ISBN 978-5-9532-0465-1.
- Некрасов Б. В. Основы общей химии. — М.: Лань, 2004. — ISBN 5-8114-0501-4.
- Спицын В. И., Мартыненко Л. И. Неорганическая химия. — М.: МГУ, 1991, 1994.
- Турова Н. Я. Неорганическая химия в таблицах. Учебное пособие. — М.: ЧеРо, 2002. — ISBN 5-88711-168-2.