Formamidă
Unelte
General
Tipărire/exportare
În alte proiecte
| Formamidă | |
 | |
 | |
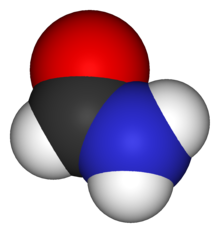 | |
| Identificare | |
|---|---|
| Număr CAS | 75-12-7 |
| ChEMBL | CHEMBL266160 |
| PubChem CID | 713 |
| Formulă chimică | CH₃NO[1] |
| Masă molară | 45 u.a.m.[1] |
| Proprietăți | |
| Densitate | 1 g/cm³[2] |
| Punct de topire | 37 de Fahrenheiti[2] |
| Presiune de vapori | 0 mm Hg[2] |
| Sunt folosite unitățile SI și condițiile de temperatură și presiune normale dacă nu s-a specificat altfel. | |
| Modifică date / text | |
Formamida (de asemenea denumită și metanamidă) este cea mai simplă amidă și anume amida acidului formic. Este un lichid incolor miscibil cu apa, cu un miros asemănător cu cel al amoniacului. Este un intermediar important în fabricarea sulfamidelor și a altor medicamente, ierbicidelor, pesticidelor și a acidului cianhidric. Este utilizat ca solvent al unor compuși ionici. [3]
Formamidele sunt compuși derivați de formamidă, cu formula generală RR′NCHO. Un reprezentat important este dimetilformamida, (CH3)2NCHO.
În trecut, sinteza formamidei se realiza prin tratarea acidului formic cu amoniac, când se obținea formiatul de amoniu. Prin încălzire, acesta trece în formamidă:[4]
De asemenea, formamida se poate obține în urma reacției de amonoliză a formiatului de etil:[5]
Procese industriale utilizate în prezent pentru sinteza chimică a formamidei implică ori carbonilarea amoniacului:[3]
Ori un procedeu în două etape de amonoliză a formiatului de metil, care la rândul său se obține din monoxid de carbon și metanol:
Formamida se descompune în monoxid de carbon și amoniac la 180 °C:
În amestecul final de reacție se regăsesc și urme de acid cianhidric și apă.
În prezența unor catalizatori acizi solizi, formamida se deshidratează la acid cianhidric:[6]