環ひずみ
有機化学において、環ひずみ(かんひずみ、英: ring strain)は、分子中の結合が異常な角度を形成する時に存在する不安定性の一種である。ひずみはシクロプロパンやシクロブタンといったC-C-C角度が約109°の理想的な値からかなりずれている小さな環について通常議論されている。高いひずみのため、これらの小さな環の燃焼熱は上昇する[1][2]。
環ひずみは角ひずみや配座ひずみ(ピッツァーひずみ)、渡環ひずみ(ファンデルワールスひずみ)の組み合わせに起因する。角ひずみの最も単純な例はシクロプロパンやシクロブタンといった小さな環状アルカンである。そのうえ、環系には緩和できない重なりひずみがしばしば存在する。
角ひずみ(バイヤーひずみ)
アルカン
アルカンにおいて、原子軌道の最適な重なりは109.5°で達成される。最も一般的な環状化合物は環内に5つあるいは6つの炭素原子を持つ[3]。アドルフ・フォン・バイヤーは、環状分子の相対的安定性を説明したバイヤーひずみ理論の発見により1905年のノーベル賞を受賞した[3]。
角ひずみは結合角が特定の化学構造において結合強度が最大となる理想的な結合角からずれた時に起こる。角ひずみは通常、非環状分子のような柔軟性を持たない環状分子に影響を与える。
角ひずみは分子を不安定化し、これは反応性の高さと燃焼熱の上昇によって明白に示される。最大の結合強度は化学結合における原子軌道の効果的な重なり合いに由来する。角ひずみの定量的評価基準はひずみエネルギーである。角ひずみとねじれひずみは組み合わさり、環状分子に影響を与える環ひずみを作り出す[3]。
- CnH2n + 3/2 n O2 → n CO2 + n H2O - ΔHcombustion
環ひずみの比較が出来るように正規化されたエネルギーはシクロアルカンのメチレン基 (CH2) 当たりのモル燃焼熱を測定することによって得られる[3]。
- ΔHcombustion per CH2 - 658.6 kJ = strain per CH2
658.6 kJ/molという値はひずみのない長鎖アルカンから得られる[3]。
| 環の大きさ | ひずみエネルギー (kcal/mol) | 環の大きさ | ひずみエネルギー (kcal/mol) | |
|---|---|---|---|---|
| 3 | 27.5 | 10 | 12.4 | |
| 4 | 26.3 | 11 | 11.3 | |
| 5 | 6.2 | 12 | 4.1 | |
| 6 | 0.1 | 13 | 5.2 | |
| 7 | 6.2 | 14 | 1.9 | |
| 8 | 9.7 | 15 | 1.9 | |
| 9 | 12.6 | 16 | 2.0 |
アルケンにおける角ひずみ
環状アルケンはsp2-混成炭素中心の変形から来るひずみを受ける。実例となるのは炭素中心がピラミッド状になっているC60である。この変形は分子の反応性を強める。角ひずみはブレット則の基礎でもある。ブレット則は極度の角ひずみが生じるため橋頭位炭素原子は二重結合を形成できない、とするものである。
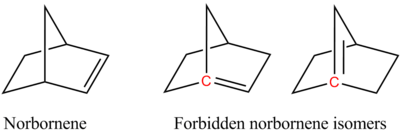
例
シクロアルカンにおいて、それぞれの炭素原子は2つの炭素原子と2つの水素原子と非極性的な共有結合を形成する。炭素原子はsp3混成であり、理想的結合角109.5°と持たなければならない。しかしながら、環構造の制限によって、この理想的角度は6員環 — いす型配座のシクロヘキサンでのみ達成される。その他のシクロアルカンでは結合角は理想的角度からずれる。シクロプロパン(炭素数3)およびシクロブタン(炭素数4)におけるC-C結合はそれぞれ60°および~90°である。
高い環ひずみを持つ分子は3員環、4員環、一部の5員環からなる。例としてはシクロプロパン、シクロプロペン、シクロブタン、シクロブテン、[1.1.1]プロペラン、[2.2.2]プロペラン、エポキシド、アジリジン、シクロペンテン、ノルボルネンが挙げられる。これらの分子の結合角はsp3およびsp2結合に必要とされる最適な正四面体型(109.5°)および正三角形型(120°)結合角よりもより狭まった結合角を持つ。そのため、結合はより高いエネルギーを持ち、p性が高くなることによって結合のエネルギーが減少する。加えて、シクロプロパンやシクロプロペン、シクロブタン、シクロブテンの環構造は非常に小さな柔軟性しかない。ゆえに、シクロプロパンの重なり形配座やシクロブタンのゴーシュ型、エクリプス型における環原子の置換基はファンデルワールス反発の形でより高い環ひずみエネルギーに寄与する。
3員環や4員環を持たないシクロアルカンもひずむことがある。これらにはシクロファンやプラトン炭化水素(キュバンなど)、ピラミッド型アルケン、環状アルキンがある。
脚注
関連項目
- ひずみ (化学)
- アルカンの立体化学