プメラー転位
プメラー転位(—てんい、Pummerer rearrangement)は、有機化学における人名反応の一種で、アルキルスルホキシドが、求電子剤の作用によりα-置換スルフィドに変わる転位反応のことを指す[1][2][3]。この反応は 1909年、R. プメラーにより最初の報告がなされた[4][5]。
無水酢酸を求電子剤として用いたプメラー転位の例を下図に示す。

反応の前後で、スルホキシドの硫黄原子が還元を受け、一方で、隣接する炭素原子が酸化を受けてアセチルオキシ化されている。この生成物を加水分解するとアルデヒド (R2CHO) が得られる[6]。
求電子剤としては、カルボン酸無水物のほか、塩化チオニルなどの求電子的なハロゲン化剤、ハロゲン化水素なども用いられる。後二者の場合では生成物はα-ハロゲン化物となる。
反応機構
無水酢酸によるプメラー転位ではまず、スルホキシド(1 と 2 の共鳴構造を持つ)のアシル化が起こる。アシル化物 3 から酢酸分子が脱離してスルホニウムイオン 4 となる。そこへ形式上、酢酸イオンが付加して生成物 5 を与える(酢酸が付加した後にプロトンが脱離してもよい)。

ほかの求核種の付加
反応中間体のスルホニウムイオンを求核剤で捕捉することができる。例えば、塩化チオニルを用いるプメラー転位では、スルホニウムイオンが形式上、塩化物イオンと反応し、塩化物を生成物として与える[7]。

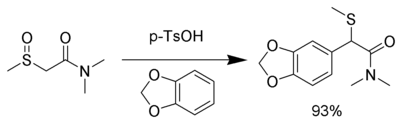
同様に、1,3-ベンゾジオキソール(下図)やベラトロール(1,2-ジメトキシベンゼン)などの電子豊富な芳香族化合物を求核剤とすることもできる[8]。