Geldanamicina
La geldanamicina è un antibiotico benzochinonico in grado di interagire con la proteina chaperon Hsp90 (Heat Shock Protein 90) inibendone la sua funzione.
| Geldanamicina | |
|---|---|
 | |
| Nome IUPAC | |
| (4E,6Z,8S,9S,10E,12S,13R,14S,16R)-13-idrossi-8,14,19-trimetossi-4,10,12,16-tetrametil-3,20,22-triossi-2-azabiciclo[16.3.1]docosa-1(21),4,6,10,18-pentan-9-il carbamato | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C29H40N2O9 |
| Massa molecolare (u) | 560.64 g/mol |
| Numero CAS | |
| PubChem | 5288382 |
| DrugBank | DBDB02424 |
| SMILES | COC1=C2CC(C)CC(OC)C(O)C(C)C=C(C)C(OC(N)=O)C(OC)C=CC=C(C)C(=O)NC(=CC1=O)C2=O |
| Proprietà chimico-fisiche | |
| Solubilità in acqua | 6,34x10-3 g/l |
| Dati farmacologici | |
| Categoria farmacoterapeutica | Antivirale, inibitore enzimatico, antibiotico |
| Indicazioni di sicurezza | |
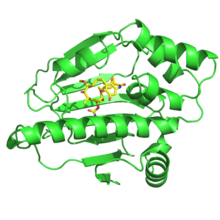
Meccanismo di azione
Le proteine clienti di HSP90 svolgono un ruolo importante nella crescita, sopravvivenza e ciclo cellulare, oltre che in processi come apoptosi, angiogenesi e oncogenesi. Il dominio N-terminale di HSP90 contiene il sito di legame per l'ATP, ed è in questa regione che avviene l'interazione tra l'enzima e l'inibitore, che compete con l'ATP per il sito attivo.[2]La geldanamicina induce la degradazione di proteine mutate o overespresse in tumori come v-Src, Bcr-Abl e p53 e ERBB2 [3] in misura preferenziale rispetto alle loro controparti cellulari normali. Questo effetto è il risultato dell'inibizione di HSP90, che normalmente interviene per mantenere il corretto ripiegamento di proteine mutate [4]. Nonostante il suo potente potenziale antitumorale questo composto presenta una discreta epatotossicità, che ha portato allo sviluppo di composti analoghi.
Biosintesi
La geldanamicina è stata originariamente scoperta in Streptomyces hygroscopicus[5] È un polichetide macrociclico sintetizzato da una polichetide sintasi (PKS) di tipo I codificata dai geni gela, gelb e gelC. La PKS viene caricata con acido 3-ammino-5-idrossibenzoico (AHBA) che viene processato attraverso cicli di estensione della catena tramite l'addizione di malonil-CoA, metilmalonil-CoA, e metossimalonil-CoA per sintetizzare la molecola precursore progeldanamicina.[6] Il precursore è sottoposto a diversi passaggi di clivaggio enzimatico e non-enzimatico per produrre la geldanamicina attiva, che comprendono idrossilazione, O-metilazione, carbamoilazione, e l'ossidazione.[7]

