Diagrama de Moeller
Herramientas
Acciones
General
Imprimir/exportar
Este artículo o sección necesita referencias que aparezcan en una publicación acreditada. Busca fuentes: «Diagrama de Moeller» – noticias · libros · académico · imágenes Este aviso fue puesto el 12 de agosto de 2022. |
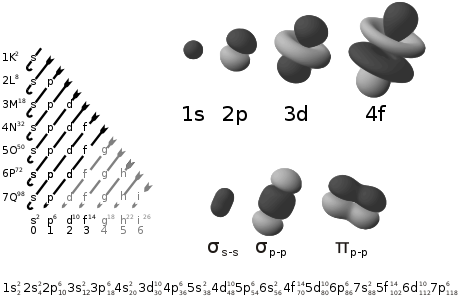
El diagrama de Moeller es una guía utilizada en química para calcular la configuración electrónica de un átomo mediante su número atómico (Z). Es aplicable en la mayoría de los elementos, con excepciones en los metales de transición y en elementos de número atómico elevado, ya que incumplen el principio de Aufbau.
Es un método gráfico y nemotécnico para aprender la regla de Madelung; esto es, cómo escribir la configuración electrónica de un elemento. Se caracteriza por trazar unas diagonales por las columnas de los orbitales, y siguiendo la dirección de la flecha se establece el orden apropiado de los mismos para un elemento.
Para comprender el diagrama se puede utilizar la siguiente tabla:
| s | p | d | f | |
|---|---|---|---|---|
Para encontrar la distribución electrónica se escriben las notaciones en forma diagonal desde arriba hacia abajo y de derecha a izquierda (seguir colores):
Obtención del diagrama de Moeller:
El Diagrama de Moeller recopila en una tabla una serie de datos que proporcionan los números cuánticos n (nivel de orbitales), l (Caracterización del orbital, s, p, d o f), m (orientación del orbital en el espacio), y s (espín, igual siempre a +1/2 ó -1/2).
Salvo en el caso de s, los valores de todos los números cuánticos se obtienen a partir del valor de n:
Así, y teniendo en cuenta que cada orbital tiene un máximo de 2 electrones[1], según el principio de exclusión de Pauli, éstos son los orbitales existentes en la configuración electrónica de los átomos, recogida de forma más sencilla en el diagrama de Moeller. Si bien hay más niveles, y, por lo tanto, más valores posibles para l, no existen en la práctica más tipos de orbitales, ya que, hasta la fecha, no ha sido descubierto ningún elemento químico cuyos átomos tengan tan elevado número de electrones como para requerir otro tipo más de orbital, algo también influido por el orden de llenado de los orbitales (véase el diagrama de Moeller, más arriba).
| Control de autoridades |
|
|---|