Chlorid platnatý
Nástroje
Obecné
Tisk/export
Na jiných projektech
| Chlorid platnatý | |
|---|---|
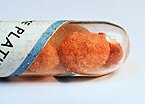 Pevný chlorid platnatý | |
 Krystalová struktura β-chloridu platnatého | |
| Obecné | |
| Systematický název | Chlorid platnatý |
| Anglický název | Platinum(II) chloride |
| Německý název | Platin(II)-chlorid |
| Sumární vzorec | PtCl2 |
| Vzhled | zelená pevná látka |
| Identifikace | |
| Registrační číslo CAS | 10025-65-7 |
| PubChem | 2770 |
| SMILES | Cl[Pt]Cl |
| InChI | InChI=1S/2ClH.Pt/h2*1H;/q;;+2/p-2 |
| Vlastnosti | |
| Molární hmotnost | 265,99 g/mol |
| Teplota tání | 581 °C |
| Teplota varu | rozkládá se |
| Hustota | 6,05 g·cm−3 |
| Rozpustnost ve vodě | nerozpustný |
| Bezpečnost | |
| [1] Nebezpečí[1] | |
Některá data mohou pocházet z datové položky. | |
Chlorid platnatý je chemická sloučenina se vzorcem PtCl2. Jde o důležitý prekurzor pro přípravu dalších sloučenin platiny. Existuje ve dvou krystalových formách, α-PtCl2 je hnědozelený, β-PtCl2 je tmavě červený, obě formy jsou nerozpustné ve vodě, ale dobře se rozpouští v kyselině chlorovodíkové za tvorby [PtCl4]2−.[2]
Strukturně je podobný chloridu palladnatému. Tyto chloridy existují v polymerní formě (α) a šesterečné (β) struktuře. β forma po zahřátí na 500 °C přechází na formu α. V obou formách jsou atomy platiny koordinovány ke čtyřem chloridovým iontům. Každý chlorid je koordinován ke dvěma atomům platiny.
β-PtCl2 lze připravit zahříváním kyseliny hexachloroplatiničité na vzduchu na teplotu 350 °C:[3]
Tato metoda se běžně používá, protože kyselinu hexachloroplatiničitou lze vyrobit přímo z kovové platiny. Vodný roztok H2PtCl6 lze také redukovat solemi hydrazinu, ale tato metoda je pracnější.
Ačkoliv PtCl2 vzniká reakcí platiny s plynným chlorem, je obtížné zabránit vzniku chloridu platiničitého (PtCl4). Ten se ale při teplotě nad 450 °C rozkládá zpět na chlorid platnatý a chlor:[4]
Většina reakcí chloridu platnatého vede k tvorbě komplexů s ligandy (L), během nich dochází k depolymeraci přerušením vazeb Cl-Pt-Cl:
Tyto reakce mohou být matoucí, přídavkem amoniaku získáme zdánlivě PtCl2(NH3)2, ale ve skutečnosti jde o Magnusovu zelenou sůl, [PtCl4][Pt(NH3)4].
Mnoho komplexů platiny nachází praktické využití, např.:[5]
Některé z těchto látek jsou zajímavé pro homogenní katalýzu v organické chemii nebo jako léčiva.[6]
V tomto článku byl použit překlad textu z článku Platinum(II) chloride na anglické Wikipedii.
| Chloridy s prvkem v oxidačním čísle II. | |
|---|---|
| Chlorid americnatý (AmCl2) • Chlorid barnatý (BaCl2) • Chlorid berylnatý (BeCl2) • Chlorid vápenatý (CaCl2) • Chlorid kademnatý (CdCl2) • Chlorid kalifornatý (CfCl2) • Chlorid kobaltnatý (CoCl2) • Chlorid chromnatý (CrCl2) • Chlorid měďnatý (CuCl2) • Chlorid dysprosnatý (DyCl2) • Chlorid einsteinatý (EsCl2) • Chlorid europnatý (EuCl2) • Chlorid železnatý (FeCl2) • Chlorid fermnatý (FmCl2) • Chlorid gallnatý (GaCl2) • Chlorid germanatý (GeCl2) • Chlorid rtuťnatý (HgCl2) • Chlorid indnatý (InCl2) • Chlorid iridnatý (IrCl2) • Chlorid mendelevnatý (MdCl2) • Chlorid hořečnatý (MgCl2) • Chlorid manganatý (MnCl2) • Chlorid molybdenatý (Mo6Cl12) • Chlorid neodymnatý (NdCl2) • Chlorid nikelnatý (NiCl2) • Chlorid nobelnatý (NoCl2) • Chlorid osminatý (OsCl2) • Chlorid olovnatý (PbCl2) • Chlorid palladnatý (PdCl2) • Chlorid polonatý (PoCl2) • Chlorid platnatý (PtCl2) • Chlorid radnatý (RaCl2) • Chlorid ruthenatý (RuCl2) • Chlorid sirnatý (SCl2) • Chlorid selenatý (SeCl2) • Chlorid samarnatý (SmCl2) • Chlorid cínatý (SnCl2) • Chlorid strontnatý (SrCl2) • Chlorid tellurnatý (TeCl2) • Chlorid titanatý (TiCl2) • Chlorid thulnatý (TmCl2) • Chlorid vanadnatý (VCl2) • Chlorid wolframnatý (WCl2) • Chlorid xenonatý (XeCl2) • Chlorid ytterbnatý (YbCl2) • Chlorid zinečnatý (ZnCl2) | |
| viz též Diborotetrachlorid (B2Cl4) • Dichlorkarben (CCl2) • Tetrachlorethylen (C2Cl4) • Tetrachlordifosfan (P2Cl4) | |