Foszforil-klorid
| foszforil-klorid | |||
 foszforil-klorid | |||
 |  | ||
 | |||
| Más nevek | foszfor-oxiklorid | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| CAS-szám | 10025-87-3 | ||
| PubChem | 24813 | ||
| ChemSpider | 23198 | ||
| EINECS-szám | 233-046-7 | ||
| ChEBI | 30336 | ||
| RTECS szám | TH4897000 | ||
| |||
| |||
| InChIKey | XHXFXVLFKHQFAL-UHFFFAOYSA-N | ||
| UNII | 9XM78OL22K | ||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | POCl3 | ||
| Moláris tömeg | 153,33 g/mol | ||
| Megjelenés | színtelen, nedves levegőn füstölgő folyadék | ||
| Szag | pungent and musty | ||
| Sűrűség | 1,645 g/cm³, liquid | ||
| Olvadáspont | 1,25 °C | ||
| Forráspont | 105,8 °C | ||
| Oldhatóság (vízben) | reagál | ||
| Oldhatóság | jól oldódik benzolban, kloroformban, szén-diszulfidban, szén-tetrakloridban | ||
| Törésmutató (nD) | 1,460 | ||
| Gőznyomás | 40 Hgmm (27 °C)[2] | ||
| Kristályszerkezet | |||
| Molekulaforma | tetraéderes | ||
| Dipólusmomentum | 2,54 D | ||
| Termokémia | |||
| Std. képződési entalpia ΔfH | -568,4 kJ/mol | ||
| Hőkapacitás, C | 84,35 J/mol K | ||
| Veszélyek | |||
| EU osztályozás | erősen mérgező (T+) ártalmas (Xn) korrozív (C) | ||
| NFPA 704 | |||
| R mondatok | R14, R22, R26, R35, R48/23 | ||
| S mondatok | (S1/2), S7/8, S26, S36/37/39, S45 | ||
| PEL | nincs[2] | ||
| LD50 | 36 mg/kg (patkány, szájon át) | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
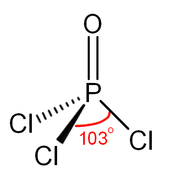
A foszforil-klorid (más néven foszfor-oxiklorid) színtelen folyadék, képlete POCl3. Nedves levegőn foszforsav és hidrogén-klorid keletkezése közben hidrolizál. Nagyléptékű ipari előállítása foszfor-triklorid és oxigén vagy foszfor-pentoxid felhasználásával történik.[3] Főként foszfofát észterek, például trikrezil-foszfát előállítására használják.
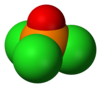
Szerkezete
A foszfátokhoz hasonlóan molekulája tetraéderes alakú,[4] benne három P−Cl kötés és egy erős P=O kettős kötés található, utóbbinak becsült kötés disszociációs energiája 533,5 kJ/mol.
Fizikai tulajdonságai
Folyadéktartománya nagyon hasonlít a vízére: olvadáspontja 1 °C, forráspontja 106 °C. Szintén a vízhez hasonló tulajdonsága autoionizációja, ennek során egyensúlyi reakcióban POCl2+,Cl− keletkezik.
Kémiai tulajdonságai
Vízzel hidrogén-klorid és foszforsav képződése közben reagál:
- O=PCl3 + 3 H2O → O=P(OH)3 + 3 HCl
A fenti reakció köztitermékeit, többek között a pirofoszforil-kloridot (P2O3Cl4) izolálták.[5]
Feleslegben levő alkoholokkal és fenolokkal kezelve foszfát észterek keletkeznek:
- O=PCl3 + 3 ROH → O=P(OR)3 + 3 HCl
Ezeket a reakciókat HCl megkötésére képes anyagok, például piridin vagy valamilyen amin jelenlétében végzik.
Lewis-bázisként is reagálhat, különböző Lewis-savakkal, például titán-tetrakloriddal adduktumokat képez:
- Cl3PO + TiCl4 → Cl3POTiCl4
Alumínium-kloriddal képzett adduktuma (POCl3·AlCl3) meglehetősen stabil, így a POCl3 felhasználható arra, hogy a reakcióelegyekből – például egy Friedel–Crafts-reakció végén – eltávolítsák az AlCl3-ot.
Lewis-sav katalizátor jelenlétében a POCl3 hidrogén-bromiddal POBr3-at képez.
Előállítása
Számos módszerrel előállítható. Elsőként Charles Adolphe Wurtz francia kémikus számolt be róla 1847-ben, ő foszfor-pentakloridot reagáltatott vízzel.[6]
Oxidációval
Ipari előállítása a foszfor-triklorid oxigénnel történő oxidációján alapul:[7]
- 2 PCl3 + O2 → 2 POCl3
Egy másik, hasonló eljárásban a foszfor-trikloridot kálium-kloráttal oxidálják:[8]
- 3 PCl3 + KClO3 → 3 POCl3 + KCl
Oxigenizálás
A foszfor-pentaklorid (PCl5) reakciója foszfor-pentoxiddal (P4O10):
- 6 PCl5 + P4O10 → 10 POCl3
A reakció egyszerűsíthető a PCl3 és P4O10 keverékének klórozásával, ami in situ hozza létre a PCl5-ot.A foszfor-pentaklorid és bórsav vagy oxálsav reakciója:[8]
További eljárások
A trikalcium-foszfát szenes redukciója klórgáz jelenlétében:[9]
Beszámoltak foszfor-pentoxid és nátrium-klorid reakciójában történő keletkezéséről is:[9]
- 2 P2O5 + 3 NaCl → 3 NaPO3 + POCl3.
Felhasználása
Egyik kereskedelmi felhasználása a foszfát észterek gyártása. A triaril-foszfátokat, például a trifenil- és trikrezil-foszfátot a PVC égésgátló és lágyító szereként használják. A trialkilfoszfátokat, például a tributil-foszfátot folyadék-folyadék extrakciós oldószerként használják, többek között a nukleáris fűtőelemek feldolgozása során.
A félvezetőiparban a POCl3-at a diffúziós eljárás foszforforrásaként alkalmazzák. A foszforral történő dópolás n-típusú félvezetőréteget hoz létre a szilícium lapok felületén.[forrás?]
Reagensként
A laboratóriumban dehidratációs reakciók reagenseként alkalmazzák, erre példa a primer amidok nitrilekké történő átalakítása:[10]
- RC(O)NH2 + POCl3 → RCN + "PO2Cl" + 2 HCl
Hasonló reakcióval egyes aril-szubsztituált amidok gyűrűzárása végezhető el a Bischler–Napieralski-reakcióban.
Ezekről a reakciókról feltételezik, hogy imidoil-kloridon keresztül játszódnak le. Egyes esetekben az imidoil-klorid a végtermék, például a piridonok és pirimidonok klórszármazékká, például 2-klórpiridinné és 2-klórpirimidinné, a gyógyszeriparban használt köztitermékekké alakíthatók.[11]
A Vilsmeier–Haack-reakcióban a POCl3 amiddal reagálva „Vilsmeier-reagenst”, klór-imínium sót hoz létre, mely azután elektronban gazdag aromás vegyületekkel reagálva – vizes feldolgozást követően – aromás aldehidekké alakítható.[12]
Jegyzetek
Fordítás
Ez a szócikk részben vagy egészben a Phosphoryl chloride című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.



