COPII
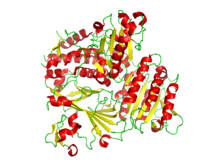 | |
| Diagrama de fitas da estrutura cristalográfica do heterodímero COPII de Sec23 e Sec24. As hélices alfa están en vermello e as follas beta están en amarelo.[1] | |
Sec23 homólogo A | |
| Identificadores | |
| Símbolo | SEC23A |
| Entrez | 856311 |
| HUGO | 10701 |
| OMIM | |
| PDB | 1M2V |
| RefSeq | NM_006364 |
| UniProt | Q15436 |
| Outros datos | |
| Locus | Cr. 14 q21.1 |
SEC24, membro A | |
| Identificadores | |
| Símbolo | SEC24A |
| Entrez | 10802 |
| HUGO | 10703 |
| OMIM | |
| PDB | 1M2V |
| RefSeq | XM_001132082 |
| UniProt | O95486 |
| Outros datos | |
| Locus | Cr. 5 q31.1 |
A COPII (/cop dous/) é un coatómero, un tipo de proteína que forma o recubrimento de vesículas celulares que transportan proteínas desde o retículo endoplasmático rugoso ao aparato de Golgi.[2][3] Este proceso denomínase transporte anterógrado, en contraste co transporte retrógrado asociado coas proteínas COPI (/cop un/). O nome "COPII" procede do inglés coat protein complex II (complexo proteico de cuberta II), que inicia o proceso de evaxinación das vesículas. As vesículas recubertas de COPII denomínanse vesículas COPII. O recubrimento ou revestimento consta de grandes subcomplexos de proteínas que están formados por catro subunidades diferentes.
Proteínas de cuberta
O complexo de recubrimento COPII está formado por dous heterodímeros proteicos (en total catro subunidades), que son:
- Heterodímero Sec23p/Sec24p
- Heterodímero Sec13p/Sec31p
Estas proteínas por si soas non poden causar a evaxinación da vesícula nin dirixir a vesícula á membrana diana correcta. Cómpre tamén a presenza de proteínas SNARE, as proteíns do cargamento e outras proteínas para que este proceso aconteza. Porén, a proteína COPII si causa as unións que forman o revestimento da vesícula, e, por tanto, orixina a súa liberación do retículo endoplasmático. O proceso exacto de como se leva a vesícula ata un lugar determinado, ou de como se determina ese lugar aínda non se coñece.
Proceso de evaxinación
A GTPase Sar1p é unha proteína que hidroliza GTP e actúa como un "interruptor" molecular que cambia entre unha forma activa unida a GTP incrustada na membrana e unha forma inactiva unida a GDP soluble.[4] A Sar1p unida a GDP inactiva é atraída ao lado citosólico do retículo endoplasmático. Sec12 é unha proteína transmembrana que se encontra no retículo endoplasmático e actúa como un factor de intercambio do nucleótido de guanina o estimular a liberación de GDP para permitir a unión no seu lugar de GTP. Agora, no estado unido a GTP, Sar1p sofre un cambio conformacional que deixa exposta unha cola hidrofóbica que pode ser inserida na bicapa lipídica, uníndoa á membrana. A Sar1p unida a membrana recruta o complexo Sec23p/24p para formar o que se coñece en conxunto como complexo de preevaxinación. O complexo de preevaxinación recruta o longo e flexible complexo Sec13p/31p. Os complexos Sec13p/31p polimerízanse no lado citosólico da membrana para formar unha estrutura reticulada convexa. A rede que se está a ensamblar causa que a membrana sobresaia cara a fóra ata que a vesícula acaba por evaxinarse. Algunhas proteínas son responsables do empaquetamento selectivo de cargamentos nas vesículas COPII. Por exemplo, Erv29p en Saccharomyces cerevisiae é necesaria para o empaquetamento do factor pro-α glicosilado.[5]
Cambios conformacionais
A COPII ten tres sitios específicos de unión nos que se poden formar complexos. A imaxe da dereita (Sed5) presenta o complexo Sec22 t-SNARE unido. Este sitio forma unións máis fortes, polo que é o máis favorecido. (Embo)

