Acide pentanoïque
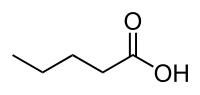
L'acide pentanoïque, ou acide méthyléthylacétique ou acide valérique, est un acide carboxylique linéaire de formule semi-développée CH3(CH2)3COOH. Il sert principalement à la synthèse d'arômes, d'adoucissantsou de produits agrochimiques. Il est également appelé acide valérique ou acide valérianique, car il a initialement été isolé des rhizomes de la valériane.
| Acide pentanoïque | |
 | |
| Identification | |
|---|---|
| Nom UICPA | acide pentanoïque |
| Synonymes | acide valérique |
| No CAS | |
| No ECHA | 100.003.344 |
| No CE | 203-677-2 |
| PubChem | 7991 |
| FEMA | 3101 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C5H10O2 [Isomères] |
| Masse molaire[1] | 102,131 7 ± 0,005 3 g/mol C 58,8 %, H 9,87 %, O 31,33 %, |
| Propriétés physiques | |
| T° fusion | −32 °C [2] |
| T° ébullition | 184 à 187 °C [2] |
| Solubilité | 40 g·l-1 (eau,20 °C) [2] |
| Paramètre de solubilité δ | 20,1 MPa1/2 (25 °C)[3]; 24,7 J1/2·cm-3/2 (25 °C)[4] |
| Masse volumique | 0,933 9 g·cm-3 à 25 °C[5] |
| T° d'auto-inflammation | 375 °C [2] |
| Point d’éclair | 87 °C [2] |
| Limites d’explosivité dans l’air | 1,6–7,3 %vol [2] |
| Thermochimie | |
| ΔfH0gaz | −491 ± 20 kJ mol−1[6] |
| ΔfH0liquide | −558,9 ± 0,7 kJ mol−1[6] |
| Précautions | |
| SGH[2] | |
| H314 et H412 | |
| SIMDUT[7] | |
   B3, D1B, E, | |
| Transport[2] | |
| Écotoxicologie | |
| DL50 | 600 mg·kg-1 (souris, oral) 1,29 g·kg-1 (souris, i.v.) 3,59 g·kg-1 (souris, s.c.) 3,59 g·kg-1 (souris, i.p.) [8] |
| LogP | 1,39 [2] |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier | |
Propriétés physico-chimiques
Il possède une odeur désagréable et caractéristique. Sa solubilité est limitée dans l'eau mais complète dans les solvants organiques communs[10].
Utilisation
Il est principalement utilisé en synthèse pour la production d'esters par réaction avec les alcools pour la fabrication d'arômes et d'adoucissants. Le sel de sodium et de calcium sont parfois utilisés comme fongicides[10].
Production et synthèse
L'acide pentanoïque est principalement produit par oxydation du pentanal en présence de dioxygène[10].


