Ácido p-toluenosulfónico
El ácido p-toluenosulfónico o ácido tosílico (TsOH) es un compuesto orgánico de fórmula CH3C6H4SO3H. Es un sólido blanco soluble en agua, alcoholes, y otros disolventes polares. El grupo 4-CH3C6H4SO2- es conocido como grupo tosilo y es abreviado a menudo como Ts o Tos.
| Ácido p-toluenosulfónico | ||
|---|---|---|
 | ||
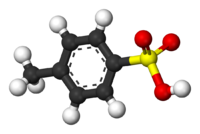 | ||
| Nombre IUPAC | ||
| ácido 4-metilbenzenosulfónico | ||
| General | ||
| Otros nombres | ácido tosílico (TsOH) PTSA | |
| Fórmula semidesarrollada | CH3C6H4SO3H | |
| Fórmula molecular | C7H8SO3 | |
| Identificadores | ||
| Número CAS | 104-15-4[1] | |
| ChEBI | 27849 | |
| ChEMBL | CHEMBL541253 | |
| ChemSpider | 5876 | |
| DrugBank | DB03120 | |
| UNII | QGV5ZG5741 | |
| KEGG | C06677 | |
| Propiedades físicas | ||
| Apariencia | blanco | |
| Masa molar | 172,20 g/mol (anhidro) 190.22 g/mol (monohidratado) g/mol | |
| Punto de fusión | 311(anhidro),[2] 376-379 (monohidratado) | |
| Punto de ebullición | 413 K (140 °C) | |
| Propiedades químicas | ||
| Acidez | -2.8 (agua),[3] | |
| Peligrosidad | ||
| Frases R | R36, R37, R38 | |
| Frases S | S26 | |
| Riesgos | ||
| Piel | Irritante de la piel | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
El TsOH es un ácido orgánico fuerte, aproximadamente un millón de veces más fuerte que el ácido benzoico. Es uno de los pocos ácidos fuertes que es sólido. También, a diferencia de algunos ácidos minerales fuertes (especialmente ácido nítrico, ácido sulfúrico y ácido perclórico), el TsOH es un ácido no oxidante.
Síntesis
El TsOH se prepara a escala industrial mediante la sulfonación de tolueno (se hace reaccionar el tolueno con ácido sulfúrico concentrado, que es una mezcla de H2SO4 y SO3, y se forma el ácido sulfónico TsOH). El electrófilo que reacciona puede ser HSO3+ o SO3.[5]
- CH3C6H5 + H2SO4H (SO3) →
- → p-CH3C6H4SO3H (TsOH) + H2O
Las impurezas comunes incluyen el ácido bencenosulfónico y el ácido sulfúrico, pero éstas no pueden eliminarse. Se hidrata con facilidad.
Ésteres tosilato

Los tosilatos son usados como agentes alquilantes debido a que el grupo tosilo es un grupo aceptor de electrones, lo que lo convierte en un buen grupo saliente. El grupo tosilo es también un grupo protector para alcoholes y aminas, por combinación del alcohol o amina con cloruro de 4-toluenosulfonilo, en un disolvente aprótico, a menudo, piridina.[6] Estos ésteres toluenosulfonato pueden someterse a un ataque nucleófilo (por reacción de sustitución nucleófila) o una eliminación. La reducción de ésteres tosilato da el hidrocarburo; así, tosilación seguida de reducción permite la desoxigenación de alcoholes.
Reacciones y usos
El ácido toluenosulfónico se usa en síntesis orgánica como un catalizador ácido "orgánico soluble". Ejemplos de distintos usos:
- Acetalización de un aldehído.[7]
- Esterificación de ácidos carboxílicos.[8]
- Transesterificación de un éster.[9]
Otros usos serían:
- El ácido p-toluenosulfónico se puede convertir en anhídrido p-toluenosulfónico por calentamiento con pentóxido de fósforo.[10]
- Cuando se calienta TsOH con ácido y agua, se lleva a cabo una reacción de hidrólisis y se forma tolueno:
- CH3C6H4SO3H + H2O → C6H5CH3 + H2SO4
Esta reacción es general para los ácidos sulfónicos derivados de grupo arilo, pero la velocidad a la que se produce depende de la estructura del ácido, la temperatura y la naturaleza del catalizador ácido. Por ejemplo el p-TsOH no se ve afectado por el ácido clorhídrico concentrado frío, pero se hidroliza cuando se calienta a 186 °C en ácido fosfórico concentrado.[11][12]
Peligros
El ácido p-toluenosulfónico siempre contiene algo de ácido sulfúrico y por lo tanto tiene riesgo de corrosividad para la piel, las membranas mucosas y los ojos. La inhalación del mismo presenta riesgo de edema pulmonar.

