Propanotiolo
kemia kombinaĵo
| Propanotiolo | ||||
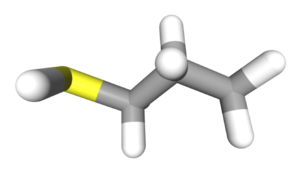 | ||||
| Bastona kemia strukturo de la Propanotiolo | ||||
 | ||||
| Tridimensia kemia strukturo de la Propanotiolo | ||||
 | ||||
| Propanotiolo kaj ĝiaj derivaĵoj nature okazas en la foliaro kaj esencaĵoj de la Allium cepa. | ||||
| Alternativa(j) nomo(j) | ||||
| ||||
| Kemia formulo | ||||
| CAS-numero-kodo | 107-03-9 | |||
| ChemSpider kodo | 7560 | |||
| Fizikaj proprecoj | ||||
| Aspekto | senkolora likvaĵo kun odoro je putra ovo | |||
| Denseco | 0,841g cm−3[1] | |||
| Fandpunkto | -113°C | |||
| Bolpunkto | 67°C | |||
| Refrakta indico | 1,437 | |||
| Ekflama temperaturo | 85 °C | |||
| Acideco (pKa) | 10,86 | |||
| Solvebleco | Akvo:1,9 g/L | |||
| Sekurecaj Indikoj | ||||
| Riskoj | R11 R20 R50/53 | |||
| Sekureco | S16 S25 S60 S61 | |||
| Pridanĝeraj indikoj | ||||
| Danĝero | ||||
| GHS Damaĝo Piktogramo |
| |||
| GHS Signalvorto | Damaĝa substanco | |||
| GHS Deklaroj pri damaĝoj | H225, H302, H315, H318, H335, H400 | |||
| GHS Deklaroj pri antaŭgardoj | P210, P233, P240, P241, P242, P243, P264, P270, P280, P301+312, P303+361+353, P305+351+338, P330, P337+313, P370+378, P403+235, P501[2] | |||
(25 °C kaj 100 kPa) | ||||
Propanotiolo aŭ tiopropanolo estas kemia kombinaĵo, apartenanta al la funkcia grupo de la tioalkoholoj, prezentanta -SH grupon ligitan al alkila grupo. Propanotiolo estas senkolora likvaĵo kun odoro je putra ovo, uzata en la fabrikado de insekticidoj, kosmetikaĵoj kaj farmaciaĵoj. Kutime ĝi estiĝas per kondensiĝa reakcio aŭ per esterigo de Fischer-Speyer. Propanotiolo estas malmulte solvebla en akvo, sed tute solvebla en alkoholo, duetila etero, kloroformo kaj plejmulto el la organikaj solvantoj. Propanotiolo reakcias kun fortaj oksidigagentoj kaj fortaj bazoj kaj posedas antifungajn kaj antibakteriajn proprecojn. Krom tio ĝi uzatas kiel konservaĵo.
Sintezoj
Sintezo 1
- Preparado per reakcio de la acetaldehido kun sulfida acido:
Sintezo 2
- Preparado per kondensiga reakcio inter propileno kaj sulfida acido:
Sintezo 3
- Preparado per agado de la propila klorido sur natria sulfido:
Sintezo 4
- Preparado per traktado de dupropila sulfido kaj sulfida acido:
Sintezo 5
- Preparado per traktado de la propilamino kaj kalia sulfido:
Sintezo 6
- Preparado per reduktigo de la dupropila sulfido:
Sintezo 7
- Preparado per interagado de la kalia etilsulfato kaj kalia hidrogenosulfido:
Reakcioj
Reakcio 1
- Reakcio kun POCl3:
Reakcio 2
- Oksidigo de tiopropanolo:
Reakcio 3
- Acida esterigo de tioalkoholoj:
Reakcio 4
- Anhidrida esterigo de tioalkoholoj:
Reakcio 5
- Reakcio kun acetila klorido:
Reakcio 6
- Intramolekula forigo de hidrogena sulfido el la tiopropanolo:
Reakcio 7
- Reakcio de tiopropanolo kun jodo:
Literaturo
- Sigma Aldrich Sigma Aldrich
- Chemical Reactions in Solvents and Melts
- Coenzyme A analogs
- Green Plants: Their Origin and Diversity
- Compendium of Food Additive Specifications
- Journal of the Institute of Brewing
- Molecular Electrochemistry of Inorganic, Bioinorganic and Organometallic Compounds
- Human Metabolome Database
Referencoj
🔥 Top keywords: Vikipedio:ĈefpaĝoSpecialaĵo:SerĉiCarles Puigdemont i CasamajóSpecialaĵo:Lastaj ŝanĝojAlgoritmo de LuhnEsperantoHarvey-saŭcoDua MondmilitoVikipedioHelpo:EnhavoUzanto:男神輿/provejoVikipedio:KontaktojKategorioVikipedio:MalgarantioPortalo:KomunumoVikipedio:DiskutejoUzanto:DominikFajliloFlava galioVikipedio:Forigendaj artikolojHiphopoVikipedio:AktualaĵojAmiotrofa lateralsklerozoSeksumadoMilena VelbaSerĉilo-optimumigoVikipedio:Bonvenon al VikipedioGiorgia MeloniBottropEjakuloPetr SepéšiDistrikto Borkenre4v1UsonoCharles Antoine Houdar de La MotteEmscher-KooperativoXXXTentacionValutoKrystyna Łuczak-Surówka