Zimtaldehyd
Zimtaldehyd (3-Phenyl-2-propenal) ist eine gelbliche, intensiv nach Zimt riechende, ölige Flüssigkeit. Er ist der Hauptaromastoff der Zimtrinde und wurde erstmals im Jahre 1834 aus Zimtöl isoliert. Zimtaldehyd ist eine organische chemische Verbindung mit der Summenformel C9H8O und zählt zur Stoffgruppe der Phenylpropanoide. Er gehört zu den Aromaten und ist ein α,β-ungesättigter Aldehyd.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||||||||||||||
| Strukturformel von trans-Zimtaldehyd | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | Zimtaldehyd | |||||||||||||||||||||
| Andere Namen | ||||||||||||||||||||||
| Summenformel | C9H8O | |||||||||||||||||||||
| Kurzbeschreibung | gelbliche, intensiv nach Zimt riechende, ölige Flüssigkeit[2] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 132,16 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand | flüssig | |||||||||||||||||||||
| Dichte | 1,05 g·cm−3 (20 °C)[2] | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Siedepunkt | 246–253 °C[2] | |||||||||||||||||||||
| Dampfdruck | ||||||||||||||||||||||
| Löslichkeit |
| |||||||||||||||||||||
| Brechungsindex | 1,6219 (20 °C)[4] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||||||||
Geschichte
Zimtaldehyd wurde 1834 von Jean-Baptiste Dumas und Eugène-Melchior Péligot aus Zimtöl isoliert und 1856 von Luigi Chiozza synthetisiert.
Vorkommen
Zimtaldehyd kommt natürlich im Zimtrindenöl (42–68 %) und Cassiaöl (bis 90 %) vor, in geringerem Maße aber auch in den Blättern des Zimtbaums und in vielen anderen ätherischen Ölen.[5][6] So kann Zimtaldehyd auch in Sellerie, Benediktenkraut, Commiphora myrrha, Feigen, Gartenhyazinthen, Lavendel (Lavandula sp), Tomaten, Äpfeln, Myrtenheiden, Balsambäumen (Myroxylon balsamum), Piment, Anis, Indischem Patschuli, Rosa damascena, Heidelbeeren, Gewürzvanille, Weinreben, dem Gewürznelkenbaum und dem Tamarindenbaum nachgewiesen werden.[7]
- Borke des Zimtbaums (Cinnamomum verum)
- Rinde des Zimtbaums (Cinnamomum verum)
- Sellerie
- Äpfel
Isomerie
Die Kohlenstoff-Kohlenstoff-Doppelbindung in der Seitenkette des Zimtaldehyds ist typischerweise trans-konfiguriert. Der isomere cis-Zimtaldehyd [Synonym: (Z)-Zimtaldehyd] hat nur eine geringe Bedeutung. Die Angaben in diesem Artikel beziehen sich nur auf den trans-Zimtaldehyd [Synonym: (E)-Zimtaldehyd].
| Isomere von Zimtaldehyd | ||
| Name | trans-Zimtaldehyd | cis-Zimtaldehyd |
| Andere Namen | (E)-Zimtaldehyd | (Z)-Zimtaldehyd |
| Strukturformel |  |  |
| CAS-Nummer | 14371-10-9 | 57194-69-1 |
| 104-55-2 (unspez.) | ||
| EG-Nummer | 604-377-8 | – |
| 203-213-9 (unspez.) | ||
| ECHA-Infocard | 100.111.079 | – |
| 100.002.922 (unspez.) | ||
| PubChem | 637511 | 6428995 |
| 307 (unspez.) | ||
| Wikidata | Q204036 | Q27161918 |
| Q60041699 (unspez.) | ||
Darstellung
Natürliche Quellen
Zimtaldehyd wird durch Wasserdampfdestillation aus der Rinde (in geringerer Qualität auch den Blättern) des Zimtbaums gewonnen.[5] Aus der Rinde des Zimtbaums (Cinnamomum verum) wird Zimtöl gewonnen, das zu 65–75 % aus Zimtaldehyd besteht.[8]
Technische Synthesen
trans-Zimtaldehyd kann analog zur Zimtsäure mittels Aldol-Kondensation aus Benzaldehyd und Acetaldehyd in 60%iger Ausbeute dargestellt werden.[9]
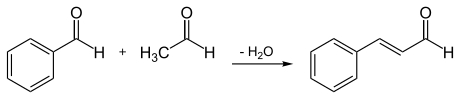
Die Darstellung gelingt auch durch Vilsmeier-Formylierung von Styrol in 30%iger Ausbeute.[10]

Der cis-Zimtaldehyd kann durch eine photochemische Isomerisierung aus der trans-Verbindung erhalten werden:[3]

Eigenschaften

(blau =negative, rot = positive Ausgleichsladung)
Physikalische Eigenschaften
Zimtaldehyd ist eine gelbliche, intensiv nach Zimt riechende, ölige Flüssigkeit, die an der Luft allmählich zu Zimtsäure oxidiert.[2] Er schmilzt bei −8 °C und siedet bei 251 °C bei Normaldruck.[2] Er löst sich sehr schlecht in Wasser (1,1 g/l bei 20 °C),[2] hingegen ist er mischbar mit Ethanol, Diethylether und Chloroform.[3]
Chemische Eigenschaften
Zimtaldehyd ist gegen Licht, Wärme, Alkalien und einige Metalle empfindlich und zeigt die üblichen Aldehyd- und Olefinreaktionen.[6]
Durch Meerwein-Ponndorf-Verley-Reduktion kann er zu Zimtalkohol in 75%iger Ausbeute reduziert werden.[11]

Durch Autoxidation an der Luft entsteht Zimtsäure.
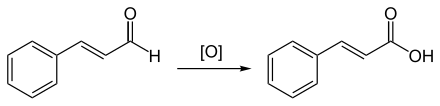
Durch stärkere Oxidationsmittel wie Kaliumpermanganat oder Ozon wird Zimtaldehyd zu Benzoesäure oxidiert.

Durch Hydrierung der Doppelbindung entsteht der Hydrozimtaldehyd.[12]

Strukturelle Verwandte

Ein Derivat ist der Coniferylaldehyd [3-(4-Hydroxy-3-methoxyphenyl)-2-propenal], der am Benzolring zusätzlich an der 4-Position eine Hydroxy- und an der 3-Position eine Methoxygruppe trägt, und damit das Substitutionsmuster wie beim Vanillin aufweist.
 |  | 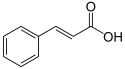 |
| Zimtalkohol | Zimtaldehyd | Zimtsäure |
Verwendung
Zimtaldehyd wird als Riechstoff in der Parfümherstellung bei der Komposition orientalischer Parfüms benutzt.[13] Es dient auch als Duftstoff in Kosmetika, z. B. in Lippenstiften, Wasch-, Reinigungsmittel, Zahnpasta und Mundwasser. Ebenso findet es als Gewürz in Nahrungsmitteln Verwendung.[5]
In reiner Form hat er sensibilisierende Eigenschaften und kann zu allergischen Hautreaktionen führen.[4] Patienten mit einer Zimtaldehydallergie reagieren häufig auch auf Perubalsam, was auf Kreuzallergien hindeutet. Die Verbindung reagiert mit nukleophilen Strukturbestandteilen von Proteinen, vor allem den Thiolgruppen des Cysteins, und kann dadurch eine Immunreaktion vom Spättyp auslösen.[5] Aufgrund seines hohen allergenen Potentials ist er ein Bestandteil des sogenannten „Duftstoff-Mix“ (engl. fragrance mix) für Epikutantests.[14][15]
Weblinks
- Eintrag zu 2-Propenal, 3-phenyl-. In: P. J. Linstrom, W. G. Mallard (Hrsg.): NIST Chemistry WebBook, NIST Standard Reference Database Number 69. National Institute of Standards and Technology, Gaithersburg MD, abgerufen am 10. September 2013.
- Riechstoff-Lexikon: Zimtaldehyd





