Hypoxanthin
Hypoxanthin ist ein natürlich vorkommendes Purinderivat und entsteht bei der Einwirkung der Xanthinoxidase auf Xanthin, obwohl der Purinabbau normalerweise so abläuft, dass Hypoxanthin durch Xanthinoxidase zu Xanthin oxidiert wird. Sehr selten bildet Hypoxanthin das Grundgerüst von Nukleinsäuren. Es ist im Anticodon der tRNA enthalten in der Form des Nukleosids Inosin.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
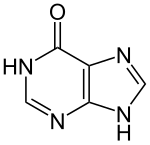 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | Hypoxanthin | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel | C5H4N4O | |||||||||||||||||||||
| Kurzbeschreibung | farblose Kristalle[1] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 136,11 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand | fest | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Löslichkeit | 25 g·l−1 in 1M Natronlauge[2] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||||||||
Vorkommen
Hypoxanthin kommt zum Beispiel im Harn in freier Form sowie auch gebunden in Nukleosiden vor.
Eigenschaften
Das Hypoxanthinmolekül weist mehrere Tautomere auf, die miteinander in einem Gleichgewicht stehen:
Vom Hypoxanthin leiten sich das Nukleosid Inosin und das Nukleotid Inosinmonophosphat ab.
Biologische Bedeutung
Hypoxanthin stellt für manche Mikroorganismen einen Wachstumsfaktor dar. Es trägt außerdem zur Färbung von Fischen bei (siehe Fischsilber). In der Hülle von Fisch-Schwimmblasen senken dichte Lagen von Hypoxanthin-Kristalliten deren Gas-Durchlässigkeit. Das an 3-Position oxidierte Hypoxanthin ist der Schreckstoff der Cypriniformes.
Historisches
Hypoxanthin wurde von Johann Joseph von Scherer in der Milz und im Herzmuskel entdeckt. Er beschrieb seine Beobachtungen 1850.[3]

