Butene
Butene (auch Butylene) sind eine Gruppe von vier isomeren Kohlenwasserstoffen mit der allgemeinen Summenformel C4H8, die über eine C=C-Doppelbindung verfügen. Sie zählen damit zu den Alkenen. Zwei der Isomere unterscheiden sich durch cis-trans-Isomerie.
Butene sind unter Standardbedingungen farblose, brennbare Gase mit einer größeren Dichte als Luft. Unter Druck lassen sich die Isomere verflüssigen. Sie wirken in höheren Konzentrationen narkotisierend und erstickend. Mit Luft bilden sie explosive Gemische.
Struktur und Eigenschaften
| Eigenschaften der Butene | ||||||||||||
| Name | But-1-en | (Z)-But-2-en | (E)-But-2-en | 2-Methylprop-1-en | ||||||||
| Andere Namen | 1-Buten n-Buten 1-Butylen α-Butylen BUTENE (INCI)[1] | cis-2-Buten (Z)-2-Buten cis-But-2-en | trans-2-Buten (E)-2-Buten trans-But-2-en | 2-Methyl-1-propen Isobuten i-Butylen | ||||||||
| Struktur | 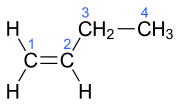 | 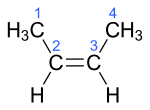 |  | 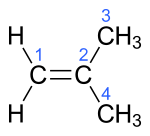 | ||||||||
| CAS-Nummer | 106-98-9 | 590-18-1 | 624-64-6 | 115-11-7 | ||||||||
| 107-01-7 (EZ)-2-Buten | ||||||||||||
| 25167-67-3 (Isomerengemisch) | ||||||||||||
| Summenformel | C4H8 | |||||||||||
| Molare Masse | 56,11 g·mol−1 | |||||||||||
| Kurzbeschreibung | farblose Gase[2] | |||||||||||
| Schmelzpunkt | −185,4 °C[3] | −138,9 °C[4] | −105,5 °C[5] | −140,4 °C[6] | ||||||||
| Siedepunkt | −6,2 °C[3] | 3,7 °C[4] | 0,9 °C[5] | −7,1 °C[6] | ||||||||
| molare Verdampfungsenthalpie am Siedepunkt | 22,07 kJ·mol−1[7] | 23,34 kJ·mol−1[7] | 22,72 kJ·mol−1[7] | 24,03 kJ·mol−1[8] | ||||||||
| Dampfdruck | 2,545 bar (20 °C) | 1,813 bar (20 °C) | 1,991 bar (20 °C) | 2,59 bar (20 °C) | ||||||||
| Untere Explosionsgrenze (20 °C / 1,013 bar)[9] | 1,2 Vol.‑% / 28 g·m3 | 1,6 Vol.‑% / 37 g·m3 | 1,6 Vol.‑% / 37 g·m3 | 1,6 Vol.‑% / 37 g·m3 | ||||||||
| Obere Explosionsgrenze (20 °C / 1,013 bar)[9] | 10,6 Vol.‑% / 252 g·m3 | 10,0 Vol.‑% / 235 g·m3 | 10,0 Vol.‑% / 235 g·m3 | 10,0 Vol.‑% / 235 g·m3 | ||||||||
| Zündtemperatur / Temperaturklasse[9] | 360 °C / T2 | 324 °C / T2 (E/Z-Isomerengemisch)[10] | 324 °C / T2 (E/Z-Isomerengemisch)[10] | 465 °C / T1 | ||||||||
| Löslichkeit | praktisch unlöslich in Wasser,[3][4][5][6] leichtlöslich in Ethanol und Ether | |||||||||||
| GHS- Kennzeichnung | aus Verordnung (EG) Nr. 1272/2008 (CLP),[11] ggf. erweitert
| aus Verordnung (EG) Nr. 1272/2008 (CLP),[12] ggf. erweitert
| aus Verordnung (EG) Nr. 1272/2008 (CLP),[13] ggf. erweitert
| aus Verordnung (EG) Nr. 1272/2008 (CLP),[14] ggf. erweitert
| ||||||||
| H-Sätze | 220‐280[3] | 220[4] | 220[5] | 220‐280[6] | ||||||||
| EUH-Sätze | keine EUH-Sätze | |||||||||||
| P-Sätze | 210‐377‐381‐403[3] | 210[4] | 210[5] | 210‐377‐381‐403[6] | ||||||||
Thermodynamische Eigenschaften
Butene sind leicht zu verflüssigende Gase, deren Anwendung und Umsetzung oft unter erhöhtem Druck als Flüssigkeit oder im überkritischen Zustand erfolgt.
| Dampf-Flüssig-Gleichgewichte | ||||
|---|---|---|---|---|
| Name | But-1-en | (Z)-But-2-en | (E)-But-2-en | 2-Methylprop-1-en |
| Dampfdruckfunktion nach Antoine | Parameter nach log10(P) = A−(B/(T+C)) (P in bar, T in K) | |||
| A | 4,24696 | 3,98744 | 4,04360 | 3,64709 |
| B | 1099,207 | 957,060 | 982,166 | 799,055 |
| C | −8,265 | −36,504 | −30,775 | −46,615 |
| Temperaturbereich | 195,6 K – 269,4 K | 203,06 K – 295,91 K | 201,70 K – 274,13 K | 216,40 K – 273 K |
| Quelle | [15] | [16] | [17] | [18] |
| Kritische Größen[19] | ||||
|---|---|---|---|---|
| Name | But-1-en | (Z)-But-2-en | (E)-But-2-en | 2-Methylprop-1-en |
| Kritische Temperatur Tc | 146,35 °C / 419,5 K | 162,35 °C / 435,5 K | 155,45 °C / 428,6 K | 144,75 °C / 417,9 K |
| Kritischer Druck pc | 40,2 bar | 42,1 bar | 41,0 bar | 40,0 bar |
| Kritisches Molvolumen Vm,c | 0,2408 l·mol−1 | 0,2338 l·mol−1 | 0,2377 l·mol−1 | 0,2388 l·mol−1 |
| Kritische Dichte ρc | 4,15 mol·l−1 | 4,28 mol·l−1 | 4,21 mol·l−1 | 4,19 mol·l−1 |
Synthese
Michael Faraday fand Butene 1825 als gasförmigen Bestandteil bei der Destillation von Erdöl (siehe auch: Flüssiggas). Butene können durch Cracken von Erdöl als Isomerengemisch gewonnen werden. Sie werden auch durch katalytische Dehydrierung von Butan bzw. Isobutan gewonnen. Die Trennung der Isomeren kann mit Hilfe von Zeolithen erfolgen.[10]
Verwendung
Durch die C–C-Doppelbindung sind sie interessante und wichtige Ausgangsstoffe für chemische Synthesen. Sie werden zur Herstellung von Verbindungen wie 2-Butanol, 2-Butanon (Ethylmethylketon) und 1,3-Butadien verwendet und sind Ausgangsstoff zur Herstellung von Kunststoffen (z. B. Butylkautschuk und Polyisobuten).[10] Als Alkylierungsmittel dienen sie z. B. zur Synthese von Zusätzen für klopffeste Treibstoffe (2,2,4-Trimethylpentan (Isooctan)). Isobuten wird zur Synthese von Methyl-tert-butylether (MTBE) bzw. Ethyl-tert-butylether (ETBE) benötigt. Auch tert-Butylester lassen sich über die Reaktion von Isobuten und (Carbon)säuren herstellen. Diese Syntheseroute bietet sich speziell dann an, wenn bei der Veresterung mit tert-Butanol als Konkurrenzreaktion dessen Dehydratisierung dominiert.
Literatur
- F.M.A. Geilen; G. Stochniol; S. Peitz; E. Schulte-Koerne: Butene, in: Ullmanns Enzyklopädie der Technischen Chemie, Wiley-VCH Verlag GmbH & Co. KGaA, Weinheim 2013; doi:10.1002/14356007.a04_483.pub3.

