Baeyer-Villiger-Oxidation
Die Baeyer-Villiger-Oxidation ist eine Reaktion in der organischen Chemie. Dabei reagiert ein Keton mit einer Percarbonsäure zum Ester[1]:

Cyclische Ketone werden dabei unter Ringerweiterung in Lactone umgewandelt.[2] Die Reaktion wird durch die Gegenwart von Lewis-Säuren, z. B. Bortrifluorid (BF3), katalytisch beschleunigt.
Die Baeyer-Villiger-Oxidation ist nach dem deutschen Chemiker Adolf von Baeyer (1835–1917) und dem Schweizer Chemiker Victor Villiger (1868–1934) benannt.
Reaktionsmechanismus
Eine besonders gut geeignete Percarbonsäure für die Baeyer-Villiger-Reaktion ist Peroxytrifluoressigsäure (2).[3]

Das Keton 1 und die Percarbonsäure 2 reagieren unter Bildung des instabilen tetraedischen Zwischenprodukts 3 mit einer schwachen O-O-Bindung. Nach heterolytischer Spaltung der O-O-Bindung wandert eine der Alkylgruppen (oben: R) zu einem O-Atom.[4] Es entsteht ein Ester 4. Neben der katalytischen Beschleunigung durch Lewis-Säuren hat der Charakter der Abgangsgruppe [oben: Trifluoracetat (5)] und die „wandernde“ Gruppe einen wesentlichen Einfluss auf die Reaktionsgeschwindigkeit.
Bei unsymmetrisch substituierten Ketonen wandert im Allgemeinen die Gruppe, welche die positive Ladung des Carbeniumions besser stabilisieren kann, falls ihre Wanderung nicht sterisch gehindert ist.
Die relative Wanderungstendenz nimmt in folgender Reihenfolge ab:[3]
tert-Alkyl > sec-Alkyl = Phenyl > prim-Alkyl > Methyl
Experimentelle Untersuchungen der Baeyer-Villiger-Oxidation von 18O-markiertem Benzophenon zeigten, dass die Carbonylgruppe des Ketons unverändert im Endprodukt (Benzoesäurephenylester) erscheint:[5]

Aldehyde
Aldehyde werden in der Regel zu Carbonsäuren oxidiert, da ein H-Atom in den meisten Fällen die größte Wanderungstendenz zeigt (für Ausnahmen siehe Dakin-Reaktion). Diese Reaktion besitzt präparativ jedoch nur eine geringe Bedeutung, da es viele andere Methoden zur Oxidation von Aldehyden zu Carbonsäuren gibt, die einfacher und atomökonomischer realisierbar sind.
Technische Anwendung
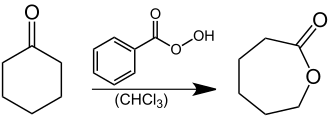
Caprolacton, ein Grundstoff zur Herstellung von Polycaprolacton, einem Kunststoff aus der Gruppe der Thermoplaste, kann technisch durch eine Baeyer-Villiger-Oxidation von Cyclohexanon mit Persäuren, wie Peressigsäure,[6] Perbenzoesäure[7] oder m-Chlorperbenzoesäure[8] hergestellt werden. Die Oxidation kann jedoch auch mittels Katalysatoren durch Sauerstoff bewerkstelligt werden.[9][10] Im Labor benutzt man Perbenzoesäure als Oxidationsmittel:[2]
Enzymatische Variante
Die Verwendung von Baeyer-Villiger-Monooxygenasen (BVMO) erlaubt die enantioselektive Synthese von chiralen Lactonen, wobei die Subklasse der Cyclohexanon-Monooxygenasen (CHMO) sich als besonders effektiv erwiesen hat. So kann z. B. 4-Methylcyclohexanon enantioselektiv (> 96 % ee) zu (S)-4-Methyl-ε-caprolacton oxidiert werden. Der Mechanismus der enzymatischen Baeyer-Villiger-Reaktion wurde näher untersucht.[11]
