2,3-Dibrom-1-propanol
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
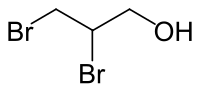 | |||||||||||||||||||
| Strukturformel ohne Stereochemie | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | 2,3-Dibrom-1-propanol | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C3H6Br2O | ||||||||||||||||||
| Kurzbeschreibung | farblose Flüssigkeit[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 217,89 g·mol−1 | ||||||||||||||||||
| Aggregatzustand | flüssig[1] | ||||||||||||||||||
| Dichte | 2,116 g·cm−3[1] | ||||||||||||||||||
| Siedepunkt | |||||||||||||||||||
| Löslichkeit | löslich in Wasser[1] | ||||||||||||||||||
| Brechungsindex | 1,559[2] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Zulassungsverfahren unter REACH | besonders besorgniserregend: krebserzeugend (CMR)[4] | ||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). Brechungsindex: Na-D-Linie, 20 °C | |||||||||||||||||||
2,3-Dibrom-1-propanol ist eine chemische Verbindung aus der Gruppe der Alkohole.
Gewinnung und Darstellung
Quelltext bearbeiten2,3-Dibrom-1-propanol kann durch Bromierung von Allylalkohol mit Brom in Gegenwart von wässrigem Lithiumbromid gewonnen werden.[5]
Die beiden Enantiomere der Verbindung erhält man durch Diazotierung der diastereomeren D-Tartrat-Salze von 2,3-Dibrompropylamin.[6]
Eigenschaften
Quelltext bearbeiten2,3-Dibrom-1-propanol ist eine brennbare, schwer entzündbare, farblose in Wasser lösliche Flüssigkeit.[1]
Die Verbindung ist ein Metabolit des Flammschutzmittels Tris(2,3-dibrompropyl)phosphat, das mutagene und karzinogene Eigenschaften besitzt. DBP ist strukturverwandt mit 1,2-Dibrom-3-chlorpropan, 1,2-Dichlorpropan und 1,3-Dichlorpropen. Ähnlich wie viele halogenierte aliphatische Alkohole wird DBP im Stoffwechsel oxidiert und dehalogeniert. Das intermediäre Epoxid wird nach Konjugation an Glutathion weiter zur Mercaptursäure metabolisiert. Durch Hydrolyse des Epoxids und sukzessive Oxidation ist auch die Bildung von Bromessigsäure und von Oxalsäure möglich. Das Glutathionkonjugat kann ebenfalls zu einem hoch reaktiven Episulfoniumion verstoffwechselt werden, wodurch eine Adduktbildung am N-7 des Guanins ermöglicht wird.[7]
Verwendung
Quelltext bearbeiten2,3-Dibrom-1-propanol wurde als Zwischenprodukt bei der Herstellung von Flammschutzmitteln, Insektiziden und Pharmazeutika verwendet. Insbesondere in den 1970er Jahren wurde es hauptsächlich zur Herstellung des Flammschutzmittels Tris(2,3-dibrompropyl)phosphat verwendet, das in Textilien eingesetzt wurde. Da die technische Produktion dieses Flammschutzmittels eingestellt wurde, ist 2,3-Dibrom-1-propanol heute nur noch in Labormengen verfügbar.[5]

