

Polyoxometaláty (zkráceně POM) jsou ionty, obvykle anionty, které obsahují tři nebo více oxyanionty přechodných kovů propojené atomy kyslíku a uzavřené do trojrozměrných struktur. Atomy kovu obvykle patří některému z prvků 6. skupiny (Mo, W), méně často prvku 5. skupiny (V, Nb, Ta), ve vysokých oxidačních číslech. Tyto ionty jsou nejčastěji bezbarvé nebo oranžové a diamagnetické. Polyoxometaláty se dělí na dvě skupiny, izopolymetaláty, obsahující pouze jeden druh kovu a oxidu, a heteropolymetaláty, složené z kovu, oxidu a oxyaniontu prvku hlavní skupiny (například fosforečnanového nebo křemičitanového). Existuje řada výjimek z tohoto dělení.[1][2]
Oxidy d0 kovů, například V2O5, MoO3 a WO3 se rozpouštějí v silně zásaditých roztocích za tvorby orthometalátů, VO 3−
4 , MoO 2−
4 a WO 2−
4 . U Nb2O5 a Ta2O5 nejsou vlastnosti roztoků při vysokých pH dobře známy, i tyto oxidy ovšem vytváří polyoxometaláty.Snížení pH vede k protonaci orthometalátů, přičemž vznikají oxido-hydroxidy, jako jsou W(OH)O −
3 a V(OH)O 2−
3 . Tyto látky kondenzují v procesu zvaném olace. Nahrazením koncových vazeb M=O, které se ve skutečnosti chovají jako trojné vazby, je vyrovnáno navýšením koordinačního čísla. Skutečnost, že nebyly pozorovány polyoxochromanové klece bývá vysvětlována malými poloměry iontů Cr6+, které nemohou zaujmout oktaedrickou koordinační geometrii.[1]
Kondenzací M(OH)O n−
3 vede k odštěpení vody a tvorbě systémů vazeb M–O–M. Rovnice tvorby hexamolybdenanů vypadá takto:[3]
Zkrácená posloupnost kondenzací u vanadičnanů vypadá takto:[1][4]
Pokud se okyselení provede za přítomnosti fosforečnanu nebo křemičitanu, tak se vytvoří heteropolymetalát; Například anion PW12O 3−
40 se skládá ze sítě tvořené dvanácti oktaedrickými wolframanovými oxyanionty rozprostírajícími se kolem fosforečnanové skupiny.
V roce 1826 byl objeven fosfomolybdenan amonný, který obsahuje anion PMo12O 3−
40 .[5]
Roku 1934 byla pomocí rentgenové krystalografie určena struktura izostrukturního fosfowolframanového aniontu; tato struktura byla po svém objeviteli nazvána Kegginova struktura.[6]
V 70. letech 20. století byly vyvinuty kvartérní amoniové soli POM.[3] Tento objev umožnil systematický výzkum bez komplikací způsobovaných hydrolytickými a acidobazickými reakcemi. Zavedení 17O NMR spektroskopie usnadnilo zjišťování struktury POM roztocích.[7]
V roce 2016 byl objeven ramazzoit, první minerál obsahující polyoxometalátový kation.[8]
Obvyklé stavební jednotky polyoxometalátů mají tvar mnohostěnů s šestikoordinovanými kovovými centry. Tyto bloky mají obvykle společné hrany a vrcholy. Koordinační čísla oxidových ligandů se liší v závislosti na jejich umístění ve struktuře. Povrchové atomy kyslíku jsou obvykle koncovými nebo dvojmůstkovými ligandy. Vnitřní kyslíkové atomy jsou většinou trojnásobně vázané nebo mají oktaedrickou geometrii.[1] POM se někdy zobrazují jako rozpustné fragmenty oxidů kovů.[7]
Polyoxometaláty lze dělit do skupin podle strukturních motivů. Iso-polyoxometaláty (isopolyanionty) mají oktaedrická kovová centra. Heteropolymetaláty vytvářejí odlišné struktury, protože centrum tvořené přechodným kovem je obvykle tetraedrické. U isopolyaniontů jsou časté Lindqvistovy a u heteropolyaniontů Kegginovy struktury.
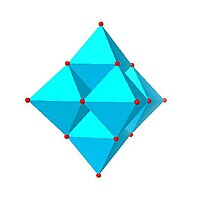 |  |  | 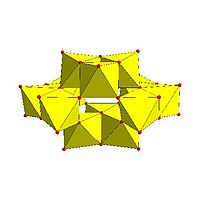 |  |
| Lindqvistův hexamolybdenan, Mo6O 2− 19 | Dekavanadičnanový anion, V10O 6− 28 | Struktura dekavanadičnanu sodného | Parawolframaman B, H2W12O 10− 42 | Mo36-polymolybdenan, Mo36O112(H2O) 8− 16 |
Polymolybdenany a polywolframany jsou, přinejmenším formálně, odvozeny od příslušných dianiontů, [MoO4]2− a [WO4]2−. Příslušná kovová centra jsou obvykle oktaedrická, někdy je tento tvar mírně narušen. Jsou také známy polymolybdenany obsahující pentagonálně bipyramidové struktury. Tyto bloky jsou součástí například molybdenových modří.[1]
Polyoxotantaličnany, polyoxoniobičnany a polyoxovanadičnany jsou odvozeny od iontů s obecným vzorcem [MO4]3−. U Nb a Ta se nejčastěji vyskytují sloučeniny se vzorcem M6 8−
16 (M = Nb, Ta), které zaujímají Lindqvistovy struktury. Tyto oktaanionty vznikají v silně zásaditých prostředích ze zásad rozpuštěných v oxidech typu M2O5, nebo u Nb také ze směsi kyseliny niobičné a vodných roztoků hydroxidů alkalických kovů. Hexatantaláty lze rovněž připravit kondenzací peroxotantaličnanů, Ta(O2) 3−
4 , v zásaditém prostředí.[9]
Tyto polyoxometaláty vykazují neobvyklé trendy co se rozpustnosti solí s alkalickými kovy týče, například jejich cesné a rubidné soli jsou lépe rozpustné než sodné a lithné soli. Opačný trend se vyskytuje u polyoxometalátů prvků 6. skupiny.[10]
Dekametaláty se vzorcem Nb10O 6−
28 jsou iszostrukturní s dekvanadičnany. Vznikají sdílením hran {MO6} oktaedrů (struktura dekawolframanu, W10O 4−
32 , obsahuje hrany i vrcholy společné vždy pro více oktaedrických wolframanových center).
Heteropolymetaláty obsahují jiné atomy než přechodné kovy. Funkci heteroatomu zde může mít řada různých prvků, nejběžnější jsou fosforečnany (PO 3-
4 ), křemičitany (SiO 4-
4 ) a arseničnany (AsO 3-
4 ).

K polyoxomolybdenanům patří také aniony molybdenových modří, mající tvary podobné kolům, a kulovité kepleráty. Shluk [Mo154(NO)14O420(OH)28(H2O)70]~20− obsahuje více než 700 atomů a velikostí odpovídá malé bílkovinné molekule. Anion má tvar pneumatiky (dutina má průměr přes 2 nm) a velmi velký vnitřní i vnější povrch.
Oxoalkoxometaláty jsou shluky obsahující oxidové i alkoxidové ligandy.[11] Obvykle v nich nejsou přítomné koncové oxoligandy. Příkladem mohou být dodekatitaničitan Ti12O16(OPri)16 (kde OPri je alkoxyskupina),[12] oxoalkoxometaláty železa[13]a železnaté[14] a měďnaté[15] Kegginovy ionty.
Koncová kyslíková centra polyoxometalátů lze někdy nahradit jinými ligandy, například S2−, Br− a NR2−.[5][16]
POM se sirnými skupinami se nazývají polyoxothiometaláty. Oxidové ionty je také možné nahradit nitrosylovými a alkoxyskupinami.[11][17]
Další skupinou polyoxometalátů jsou polyfluoroxometaláty.[18]
Je známo několik organicko-anorganických materiálů obsahujících POM jádra,[19][20][21]
Rozdílné struktury POM lze ukázat na iontu CeMo12O 8−
42 , který se skládá z osmistěnů se společnými stěnami a atomy Mo ve vrcholech dvacetistěnu.[22]
POM mají využití jako složky katalyzátorů organických oxidací.[23][24]
Velké rozpětí struktury, velikost a složení polyoxometalátů vede k mnoha různým vlastnostem a využitím těchto látek, příklady jsou tyto:
{{Cite journal}} označená jako k „pouze dočasnému použití“.{{Cite journal}} označená jako k „pouze dočasnému použití“.{{Cite journal}} označená jako k „pouze dočasnému použití“.{{Cite journal}} označená jako k „pouze dočasnému použití“.V tomto článku byl použit překlad textu z článku Polyoxometalate na anglické Wikipedii.