Bromid titaničitý
Bromid titaničitý, TiBr4, je oranžová až hnědá krystalická látka.[1] Jde o nejtěkavější bromid přechodného kovu. Jeho vlastnosti se pohybují mezi chloridem a jodidem titaničitým. Je diamagnetický, což odpovídá d0 konfiguraci titaničitého kationtu.
| Bromid titaničitý | |
|---|---|
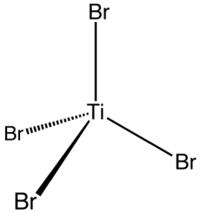 Strukturní vzorec bromidu titaničitého | |
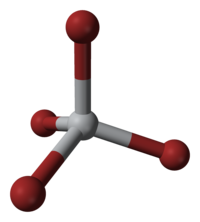 Kuličkový model bromidu titaničitého | |
| Obecné | |
| Systematický název | Bromid titaničitý |
| Anglický název | Titanium tetrabromide |
| Německý název | Titan(IV)-bromid |
| Sumární vzorec | TiBr4 |
| Vzhled | oranžovo-hnědé krystaly |
| Identifikace | |
| Registrační číslo CAS | 7789-68-6 |
| SMILES | [Ti](Br)(Br)(Br)Br |
| InChI | InChI=1S/4BrH.Ti/h4*1H;/q;;;;+4/p-4 |
| Vlastnosti | |
| Molární hmotnost | 367,483 g/mol |
| Teplota tání | 39 °C |
| Teplota varu | 230 °C |
| Hustota | 3,25 g.cm−3 |
| Rozpustnost ve vodě | hydrolyzuje |
Některá data mohou pocházet z datové položky. | |
Příprava a struktura
Lze ho připravit několika metodami, přímou reakcí z prvků, bromací oxidu v přítomnosti uhlíku (analogie Krollova procesu) nebo bromací chloridu titaničitého:
- Ti + 2 Br2 → TiBr4
- TiO2 + 2 C + 2 Br2 → TiBr4 + 2 CO
- 3 TiCl4 + 4 BBr3 → 3 TiBr4 + 4 BCl3
Má tetraedrickou geometrii.[1]
Reakce
Vytváří adukty typu TiBr4(THF)2 a [TiBr5]−.[2] S objemnými ligandy, např. 2-methylpyridinem, vytváří pětikoordinované adukty. TiBr4(2-MePy) má tvar trigonální bipyramidy, pyridinový ligand je v ekvatoriální rovině.[3]
Využívá se jako Lewisova kyselina v organické syntéze.[4]
Bromid a chlorid titaničitý spolu reagují za vzniku směsi halogenidů TiBr4−xClx (x = 0–4). Přesný mechanismus reakce není znám, ale pravděpodobně dochází ke vzniku dimerního meziproduktu.[5]
Bezpečnost
Bromid titaničitý reaguje prudce s vodou za vývoje bromovodíku.[6]
Odkazy
Reference
V tomto článku byl použit překlad textu z článku Titanium tetrabromide na anglické Wikipedii.
Externí odkazy
 Obrázky, zvuky či videa k tématu Bromid titaničitý na Wikimedia Commons
Obrázky, zvuky či videa k tématu Bromid titaničitý na Wikimedia Commons
