PAH (gen)
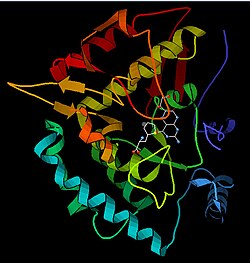
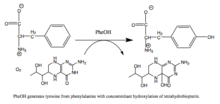
Fenilalanin-hidroksilaza (PAH) (EC 1.14.16.1) je enzim koji katalizira hidroksilaciju aromatskog bočnog lanca fenilalanina, za stvaranje tirozina. PAH je jedan od tri člana biopterin-ovisnih hidrolaznih aromatskih aminokiselina, klase monooksigenaza, koja za katalizu koristi tetrahidrobiopterin (BH4, pteridinski kofaktor) i gvožđe bez hema. Tokom reakcije, molekulni kisik se heterolitki cijepa uz uzastopnu inkorporaciju jednog atoma kisika u BH 4 i supstrat fenilalanina.[5][6] Kod ljudi, mutacije u kodirajućem genu, PAH , mogu dovesti do metaboličkog poremećaja zvanog fenilketonurija.
 |
Enzimski mehanizam
Smatra se da se reakcija odvija u sljedećim koracima:
- formiranje mosta Fe (II)-O-O-BH4.
- heterolitičko cijepanje O-O veze, kako bi se dobio feril-okso hidroksilacijski međuprodukt Fe (IV) = O
- napad na Fe(IV)=O da hidroksilira fenilalaninski supstrat u tirozin.[7]

Formiranje i rascjep gvožđe-peroksipterinskog mosta: Iako dokazi snažno podržavaju da je Fe(IV)=O hidroksilirajući intermedijar,[8] mehanički detalji koji su u osnovi formiranja mosta Fe(II)-O-O-BH4 prije heterolitnog cijepanja i dalje su kontroverzni. Predložena su dva puta na osnovu modela koji se razlikuju po blizini gvožđa do kofaktora pterina i broju molekula vode za koje se pretpostavlja da su tokom katalize koordinirane gvožđem. Prema jednom modelu, kompleks gvožđe-dioksida je inicijalno formiran i stabiliziran kao rezonantni hibrid Fe2+O2 i Fe3+O2– . Aktivirani O2 zatim napada BH4, tvoreći prijelazno stanje koje karakterizira razdvajanje naboja između pterinskog prstena s nedostatkom elektrona i elektronom bogatih vrsta kisika.[9] Kasnije se formira most Fe(II)-O-O-BH4. S druge strane, formiranje ovog mosta modelirano je pretpostavljajući da se BH4 nalazi u prvoj koordinacijskoj ljusci gvožđa i da ono nije koordinirano ni s jednom molekulom vode. Ovaj model predviđa drugačiji mehanizam, koji uključuje radikal pterina i superoksid, kao kritične međuprodukte.[10] Kad se formira, Fe(II)-O-O-BH4, most se razgrađuje putem heterolitskog cijepanja O-O veze na Fe(IV)=O i 4a-hidroksitetrahidrobiopterin; stoga je molekulski kisik izvor oba atoma kisika koji se koriste za hidroksilaciju pterinskog prstena i fenilalanina.

Hidroksilacija fenilalanina pomoću feril-okso međuproizvoda: Budući da mehanizam uključuje Fe(IV)=O (za razliku od peroksipterina) hidroksilacijski intermedijer, oksidacija kofaktora BH4 i hidroksilacija fenilalanina može se odvojiti, što rezultira neproduktivnom potrošnjom BH4 i stvaranjem H2O2.[7] Međutim, kada je produktivan, Fe(IV)=O međuprodukt dodaje se fenilalaninu u reakciji elektrofilne aromatske supstitucije koja reducira gvožđe iz feri u stanje fero.[7] Iako je u početku bio predložen arenski oksid ili radikalni međuprodukt, analize srodnih triptofan– i tirozin-hidroksilaze sugerirale su da se reakcija umjesto toga odvija kroz kationski intermedijer koji zahtijeva da se Fe(IV)=O koordinira s vodenim ligandom, a ne s hidrokso-grupom.[7][11] Ovaj kationski intermedijer naknadno prolazi 1,2-hidridni NIH pomak, dajući dienonski međuprodukt koji se zatim tautomerizira u tvorbu tirozinskih proizvoda.[12] Kofaktor pterina regenerira se hidratacijom karbinolaminskog produkta PAH u kinonoid-dihidrobiopterin (qBH2), koji se zatim reducira na BH4.[13]
Regulacija enzima
Predlaže se da se PAH koristi morfinski model alosterne regulacije.[14][15]
Sisarski PAH postoji u ravnoteži koja se sastoji od tetramera dvije različite arhitekture, s jednim ili više dimernih oblika kao dijelom ravnoteže. Ovo ponašanje je u skladu s disocijativnim alosternim mehanizmom.[15]
Mnoge studije sugeriraju se sisarski PAH ponaša usporedivo s porfobilinogen-sintazom (PBGS), pri čemu se navodi da različiti faktori, poput pH i vezivanja liganda, utiču na aktivnost enzima i stabilnost proteina.[15]
Aminokiselinska sekvenca
Dužina polipeptidnog lanca je 452 aminokiseline, a molekulska težina 51 862Da.[16]
| 10 | 20 | 30 | 40 | 50 | ||||
|---|---|---|---|---|---|---|---|---|
| MSTAVLENPG | LGRKLSDFGQ | ETSYIEDNCN | QNGAISLIFS | LKEEVGALAK | ||||
| VLRLFEENDV | NLTHIESRPS | RLKKDEYEFF | THLDKRSLPA | LTNIIKILRH | ||||
| DIGATVHELS | RDKKKDTVPW | FPRTIQELDR | FANQILSYGA | ELDADHPGFK | ||||
| DPVYRARRKQ | FADIAYNYRH | GQPIPRVEYM | EEEKKTWGTV | FKTLKSLYKT | ||||
| HACYEYNHIF | PLLEKYCGFH | EDNIPQLEDV | SQFLQTCTGF | RLRPVAGLLS | ||||
| SRDFLGGLAF | RVFHCTQYIR | HGSKPMYTPE | PDICHELLGH | VPLFSDRSFA | ||||
| QFSQEIGLAS | LGAPDEYIEK | LATIYWFTVE | FGLCKQGDSI | KAYGAGLLSS | ||||
| FGELQYCLSE | KPKLLPLELE | KTAIQNYTVT | EFQPLYYVAE | SFNDAKEKVR | ||||
| NFAATIPRPF | SVRYDPYTQR | IEVLDNTQQL | KILADSINSE | IGILCSALQK | ||||
| IK |
- Simboli
Struktura
Monomer PAH (51,9 kDa) sastoji se od tri različita domena: regulatornog N-terminalnog (ostaci 1–117) koji sadrži Phe-vezujuću ACT poddomeni, katalitskog domena (ostaci 118-427) i domena C-terminala (ostaci 428–453), odgovornih za oligomerizaciju identičnih monomera. Provedena je opsežna kristalografska analiza, posebno na katalitskom domenu koordiniranom pterinom i gvožđem, kako bi se ispitalo aktivno mjesto. Određena je i struktura N-terminalnog regulatornog domena, a zajedno s riješenom strukturom homolognog C-terminalnog domena tetramerizacije tirozin-hidroksilaze, a predložen je i strukturni model tetramernog PAH-a.[13] Using X-ray crystallography, the structure of full-length rat PAH was determined experimentally and showed the auto-inhibited, or resting-state form of the enzyme.[17] Oblik stanja mirovanja (RS-PAH) arhitektonski se razlikuje od aktiviranog oblika (A-PAH).[18] Još uvijek nedostaje cjelovita struktura A-PAH-a, ali je utvrđeno Phe stabilizirano sučelje ACT-ACT, koje je karakteristično za A-PAH i predložen je strukturni model A-PAH na osnovu analize SAXS-a.[19][20]
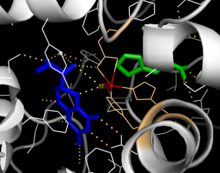
Katalitski domen
Riješene kristalne strukture katalitskog domena ukazuju na to da se aktivno mjesto sastoji od otvorenog i prostranog džepa obloženog prvenstveno hidrofobnim ostacima, iako su prisutna i tri ostatka glutaminske kiseline, dva histidina i tirozin koji vežu gvožđe.[13] Postoje kontradiktorni dokazi o koordinacijskom stanju gvožđevog atoma i njegovoj blizini BH4 unutar aktivnog mjesta. Prema kristalografskoj analizi, Fe(II) je koordiniran vodom, His285, His290 i Glu330 (aranžman trijade 2-his-1-karboksilatoliki) sa oktaedarskom geometrijom.[21] Uključivanjem analoga Phe u kristalnu strukturu, mijenja se i gvožđe iz šesto– do petokoordiniranog stanja koje uključuje jednu molekulu vode i dvozubu koordinaciju do Glu330 i otvaranje mjesta za vezanje kisika. BH4 se istodobno pomiče prema atomu gvožđa, iako pterinski kofaktor ostaje u drugoj koordinacijskoj sferi.[22] S druge strane, konkurentski model zasnovan na NMR i analizama molekulskog modeliranja sugerira da su sve koordinirane molekule vode prisiljene napustiti aktivno mjesto tokom katalitskog ciklusa, dok BH4 postaje izravno koordiniran gvožđem.[23] Kao što je gore navedno, rješavanje ove razlike bit će važno za utvrđivanje tačnog mehanizma PAH katalize.
N-terminalno regulatorno područje
Regulatorna priroda N-terminalnog domena (ostaci 1–117) data je njegovom strukturnom fleksibilnošću.[24] Analiza izmjene vodik/deuterij pokazuje da alosterno vezivanje Phe globalno mijenja konformaciju PAH, tako da je aktivno mjesto manje zagueno, jer je sučelje između regulatornih i katalitskih domena sve izloženije rastvaraču.[24][25][26] Ovo zapažanje je u skladu s kinetičkim studijama, koje pokazuju početno nisku stopu stvaranja tirozina za PAH cijele dužine. Ovo vrijeme kašnjenja se ne primjećuje za krnji PAH bez N-terminalnog domena ili ako je enzim pune dužine prethodno inkubiran s Phe.
Delecija domena N-terminala također eliminira vrijeme kašnjenja i povećava afinitet za Phe gotovo dvostruko; ne primjećuje se razlika u Vmax ili Km za kofaktor tetrahidrobiopterina.[27] Dodatne propise pruža Ser16; fosforilacija ovog ostatka ne mijenja konformaciju enzima, ali smanjuje koncentraciju Phe potrebnu za alosteričku aktivaciju.[26] Ovaj N-terminalni regulatorni domen nije primijećena u bakterijskih PAH-a, ali pokazuje značajnu strukturnu homologiju sa regulatornim domenom fosfogilcerat-dehidrogenaza, enzima u biosintetskom putu serina.[26]
Tetramerizacijski domen
Prokariotski PAH je monomerni, dok eukariotski postoji u ravnoteži između homotetramernih i homodimernih oblika.[7][13] Interfejs dimerizacije sastoji se od petlji povezanih sa simetrijom koje povezuju identične monomere, dok se preklapajući C-terminalni domen tetramerizacije posreduje u udruživanju konformacijski različitih dimera, koje karakterizira različita relativna orijentacija katalitskog i tetramerizacijskog domena (Flatmark, Erlandsen). Rezultirajuće izobličenje simetrije tetramera očito je u diferencijalnoj površini sučelja dimerizacije i razlikuje PAH od tetramerno simetrične tirozin-hidroksilaze.[13] Predložen je mehanizam zamjene tetramernog domena iz dimernog, u kojima alfa-heliksi C-terminala međusobno mijenjaju svoju konformaciju oko fleksibilnog područja šarki sa pet ostataka sa C-terminalom, kako bi formirale strukturu uprede zavojnice, pomičući ravnotežu prema tetramernom obliku.[7][13][28] Iako su i homodimerni i homotetramerni oblici PAH katalitski aktivni, ova dva pokazuju različitu kinetiku i regulaciju. Osim smanjene katalitske učinkovitosti, dimer ne pokazuje pozitivnu kooperativnost prema L-Phe (koji pri visokim koncentracijama aktivira enzim), što sugerira da L-Phe alosterno regulira PAH, utičući na interakciju dimer-dimer.[28]
Biološka funkcija
PAH je kritični enzim u metabolizmu fenilalanina i katalizira korak ograničavanja brzine u njegovom potpunom katabolizmu do ugljik-dioksida i vode.[13][29] Regulacija protoka kroz puteve povezane s fenilalaninom kritična je u metabolizmu sisara, što dokazuje toksičnost visokih koncentracija ove aminokiseline u plazmi zabilježena u fenilketonuriji (vidi dolje). Glavni izvor fenilalanina su uneseni proteini, ali relativno malo ovog bazena koristi se za sintezu proteina.[29] Umjesto toga, većina unesenog fenilalanina se katabolizira kroz PAH u oblik tirozin; dodavanje hidroksilne grupe omogućava da se benzenski prsten razbije u narednim katabolitskim koracima. Transaminacija u fenilpiruvat, čiji se metaboliti izlučuju urinom, predstavlja još jedan put prometa fenilalanina, ali prevladava katabolizam putem PAH-s.[29]
Kod ljudi, ovaj enzim se eksprimira i u jetri i u bubrezima, a postoje neke indicije da se u tim tkivima može različito regulirati.[30] PAH je neobičan među hidroksilazama aromatskih aminokiselina po svom učešću u katabolizmu; tirozin i triptofan-hidroksilaza , s druge strane, primarno se eksprimiraju u centralnom nervnom sistemu i katalizuju korake koji ograničavaju brzinu u biosintezi neurotransmitera/hormona.[13]
Klinički značaj
Nedostatak aktivnosti PAH-a zbog mutacija u PAH-u uzrokuje hiperfenilalaninemiju (HPA), a kada se razina fenilalanina u krvi poveća iznad 20 puta normalne koncentracije, dolazi do metaboličke bolesti fenilketonurija (PKU).[29] PKU je i genotipski i fenotipski heterogen: identificirano je preko 300 različitih patogenih varijanti, od kojih većina odgovara misens mutacijama koje se preslikavaju u katalitski domen.[13][21] Kada je kohorta identificiranih mutanata PAH eksprimirana u rekombinantnim sistemima, enzimi su pokazali promijenjeno kinetičko ponašanje i/ili smanjenu stabilnost, u skladu sa strukturnim mapiranjem ovih mutacija i na katalitski i na tetramerizacijski domen enzima.[13] BH4 4 primijenjen je kao farmakološki tretman i pokazano je da smanjuje razinu fenilalanina u krvi za segment pacijenata s PKU-om, čiji su genotipovi dovode do neke zaostale aktivnosti PAH -a, ali nemaju nedostatak u sintezi ili regeneraciji BH44. Kontrolne studije ukazuju na to da u slučaju određenih PAH mutanata, višak BH44 djeluje kao farmakološki šaperon za stabilizaciju mutiranih enzima s poremećenim sastavom tetramera i povećanom osjetljivošću na proteolitsko cijepanje i agregaciju.[31] Mutacije koje su identifikovane u lokusu PAH dokumentovane su u bazi poznatih fenilalanin hidroksilaze (PAHdb), [1].
Budući da fenilketonurija može uzrokovati nepovratna oštećenja, imperativ je da se nedostaci u fenilalanin-hidroksilazi utvrde u ranom razvoju. U početku je to učinjeno pomoću testa inhibicije bakterija poznatog kao Guthriejev test. Sada je PKU dio skrininga novorođenčadi u mnogim zemljama, a povišene razine fenilalanina se identificiraju ubrzo nakon rođenja mjerenjem tandemskom masenom spektrometrijom. Stavljanjem osoba na dijetu sa niskim sadržajem fenilalanina, visokim tirozina, može se spriječiti dugotrajno oštećenje njihovog razvoja.
Srodni enzimi
Fenilalanin-hidroksilaza je usko povezana sa dva druga enzima:
- triptofan-hidroksilaza (EC broj 1.14.16.4), koji kontrolira nivo serotonina u mozgu i gastrointestinalnom traktu
- tirozin-hidroksilaza (EC broj 1.14.16.2), koji kontrolira nivoe dopamina, epinefrina i norepinefrina u mozgu i srži nabubrežnih žlijezda.
Tri enzima su homologna, odnosno smatra se da su nastala iz iste iste drevne hidroksilaze.
Reference
Dopunska literatura
Vanjski linkovi
- GeneReviews/NCBI/NIH/UW entry on Phenylalanine Hydroxylase Deficiency
- Locus-specific database of the human phenylalanine hydroxylase gene variants
- Molecule of the Month: Phenylalanine Hydroxylase Arhivirano 16. 10. 2015. na Wayback Machine
- P00439
Šablon:Modulatori metabolizma monoamina